Kurze Zusammenfassung: Die digitale Transformation in der Zell- und Gentherapie nutzt fortschrittliche Fertigungstechnologien, KI/ML-Plattformen, digitale Zwillinge und integrierte Datensysteme, um die Entwicklungszeiten zu beschleunigen, die Produktqualität zu verbessern, die Ergebnisse für die Patienten zu steigern und die Produktion von autologen zu allogenen Therapien zu skalieren. Laut FDA-Leitfaden lösen diese Innovationen kritische Herausforderungen bei der Herstellung und gewährleisten gleichzeitig die Einhaltung von Vorschriften und die Zuverlässigkeit der Lieferkette.
Zell- und Gentherapien haben sich von experimentellen Behandlungen zur kommerziellen Realität entwickelt. Die Skalierung dieser personalisierten Arzneimittel stellt jedoch beispiellose Herausforderungen in Bezug auf Herstellung, Regulierung und Logistik dar.
Die digitale Transformation bietet Lösungen. Vom KI-gesteuerten Patientenabgleich bis hin zu digitalen Zwillingen, die das Ansprechen auf die Behandlung vorhersagen, verändert die Technologie jede Phase der CGT-Wertschöpfungskette.
Hier erfahren Sie, wie die digitale Innovation die Entwicklung, Herstellung und Bereitstellung von Zell- und Gentherapien vorantreibt - und was dies für Patienten und Anbieter bedeutet.
Die CGT-Marktlandschaft und die digitalen Imperative
Schätzungen zufolge wird der Markt für Zell- und Gentherapie bis 2030 weltweit $93,78 Milliarden erreichen. Dieses explosive Wachstum schafft dringende operative Anforderungen.
Herkömmliche papierbasierte Arbeitsabläufe können nicht mithalten. Manuelle Prozesse führen zu Fehlern, verlangsamen die Produktionszyklen und gefährden die Datenintegrität - kritische Probleme bei der Herstellung von patientenspezifischen Therapien mit engen Zeitvorgaben.
Die FDA hat diese Herausforderungen erkannt. Mit ihrem Advanced Manufacturing Technologies Designation Program fördert die Behörde die frühzeitige Einführung von Technologien, die die Zuverlässigkeit der Herstellung verbessern und die Entwicklungszeiten für Arzneimittel und biologische Produkte optimieren.
Die digitale Transformation stellt sich den zentralen Herausforderungen der CGT:
- Komplexe Koordinierung der Lieferkette zwischen Sammelstellen, Produktionsstätten und Behandlungszentren
- Aufrechterhaltung der Identitäts- und Überwachungskette für autologe Produkte
- Qualitätsüberwachung und Freigabetests in Echtzeit
- Dokumentation zur Einhaltung von Vorschriften und Prüfpfade
- Terminplanung für Patienten und Verwaltung des Zeitplans von Vene zu Vene
Es steht viel auf dem Spiel. Selbst bei vielversprechenden Therapien sind die Raten der Behandlungsausfälle nach wie vor beträchtlich. Die CD19-CAR-Therapie erreicht bei hämatologischen Krebserkrankungen Remissionsraten von 70-90%, doch viele Patienten erleiden aufgrund von Antigen-Downregulation und Tumorumgehungsmechanismen schließlich einen Rückfall.
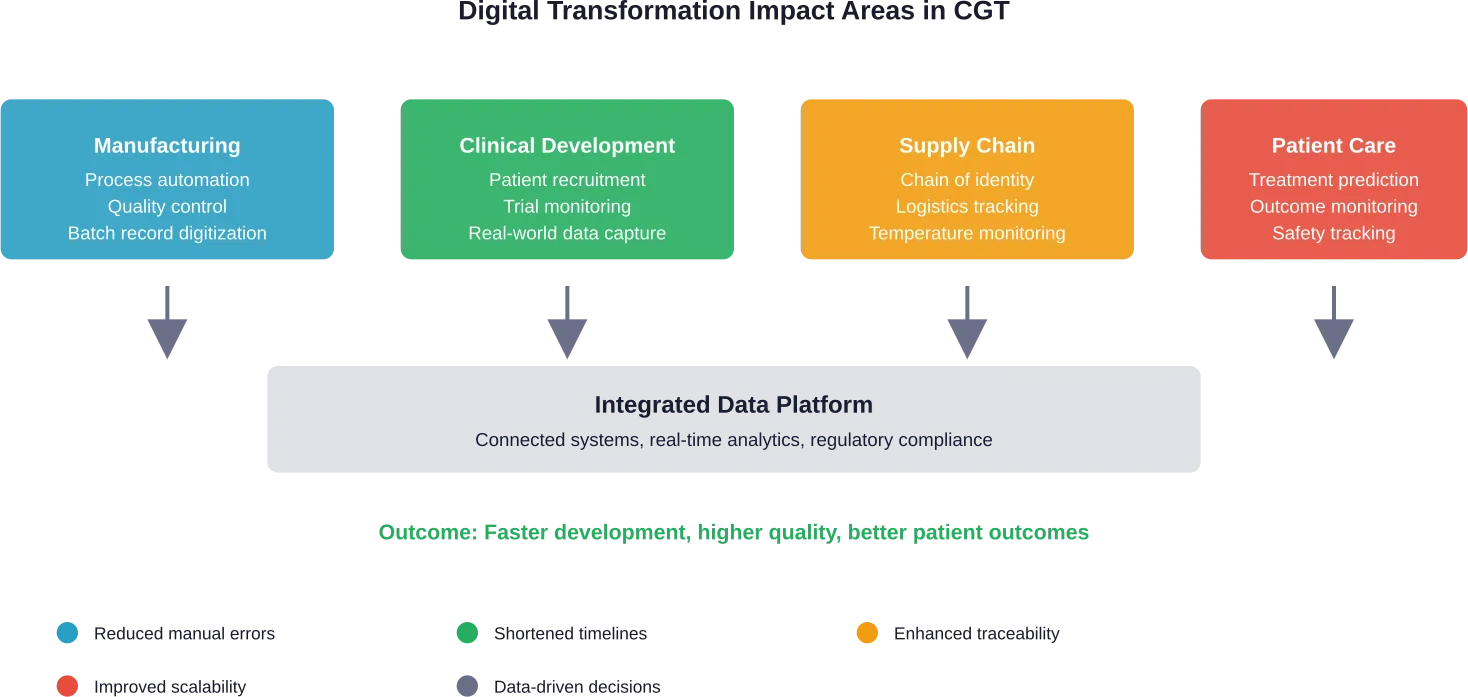
Fortschrittliche Fertigungstechnologien verändern die Produktion
Die FDA definiert fortschrittliche Fertigung als “Sammelbegriff für neue Technologien zur Herstellung von Medizinprodukten, die die Qualität von Arzneimitteln verbessern, Engpässe bei der Versorgung mit Medikamenten beheben und die Markteinführung beschleunigen können”.”
Speziell für CGT umfasst die fortschrittliche Fertigung die kontinuierliche Verarbeitung, Automatisierungsplattformen, Prozessanalysetechnologie und Qualitätsüberwachungssysteme in Echtzeit.
Elektronische Chargenprotokolle und Prozessautomatisierung
Das Ersetzen von papierbasierten Chargenprotokollen ist ein grundlegender Schritt zur digitalen Transformation. Elektronische Chargenprotokolle eliminieren Transkriptionsfehler, bieten Prozesstransparenz in Echtzeit und erstellen automatisch eine revisionssichere Dokumentation.
Führende Unternehmen berichten von erheblichen Vorteilen:
- Verkürzte Fertigungszyklen durch automatisierte Workflow-Übergänge
- Verbesserte Datenintegrität durch elektronische Unterschriften und Zeitstempelprüfung
- Schnellere Chargenfreigabe durch integrierte Qualitätsprüfungsprozesse
- Bessere Zusammenarbeit zwischen Produktionsstätten und Sponsoren
Eine erfolgreiche Implementierung erfordert jedoch mehr als nur die Bereitstellung von Software. Unternehmen müssen Arbeitsabläufe umgestalten, Mitarbeiter schulen und Systeme in den Bereichen Qualität, Fertigung und Regulierung integrieren.
Systeme für die Identitätskette und die Produktkette
Autologe Therapien erfordern die absolute Gewissheit, dass das richtige Produkt den richtigen Patienten erreicht. Digitale Identitätsketten-Systeme nutzen biometrische Verifizierung, RFID-Tracking und Barcode-Scanning, um die Rückverfolgbarkeit des Produkts von der Entnahme bis zur Infusion zu gewährleisten.
Diese Systeme lassen sich mit Planungsplattformen, Logistikanbietern und Krankenhausinformationssystemen integrieren und schaffen so eine durchgängige Transparenz, während gleichzeitig manuelle Überprüfungsschritte, die die Produktionszeiten verlangsamen, reduziert werden.
Prozessanalytische Technologie und Echtzeit-Freigabe
Herkömmliche Qualitätsprüfungen erfolgen an diskreten Chargenendpunkten. Prozessanalytische Technologie ermöglicht die kontinuierliche Überwachung kritischer Qualitätsmerkmale während der Produktion.
Die Datenerfassung in Echtzeit ermöglicht eine schnellere Entscheidungsfindung und identifiziert Abweichungen, bevor sie die Produktqualität beeinträchtigen. Einige fortschrittliche Einrichtungen führen Freigabetests in Echtzeit durch, bei denen kontinuierliche Überwachungsdaten die Endprodukttests ersetzen, wodurch sich die Freigabezeiträume drastisch verkürzen.
Digitale Zwillinge und KI-gesteuerte Behandlungsoptimierung
Die Technologie des digitalen Zwillings schafft virtuelle Nachbildungen biologischer Systeme und ermöglicht Simulationen und Vorhersagen vor physischen Eingriffen. Bei der Zell- und Gentherapie arbeiten digitale Zwillinge auf mehreren Ebenen.
Digitale Zwillinge auf Patientenebene
In medizinischen Fachzeitschriften veröffentlichte Forschungsergebnisse zeigen, dass digitale Zwillinge die Ergebnisse von CAR-T-Zelltherapien vorhersagen können, indem sie genomische Daten, Bildgebungsergebnisse, Informationen von am Körper getragenen Sensoren und klinische Aufzeichnungen in Multiskalensimulationen integrieren.
Diese patientenspezifischen Modelle helfen den Ärzten:
- Vorhersage des Ansprechens auf die Behandlung auf der Grundlage individueller Tumormerkmale und Immunprofile
- Optimierung der Dosierungsstrategien, um Wirksamkeit und Toxizitätsrisiken gegeneinander abzuwägen
- Ermittlung von Patienten, die am ehesten von bestimmten Therapieansätzen profitieren
- Überwachung des Ansprechens auf die Behandlung und Erkennung früher Rückfall-Signale
Algorithmen des maschinellen Lernens, die auf historischen Patientendaten trainiert wurden, verbessern die Vorhersagegenauigkeit im Laufe der Zeit. Mit wachsenden Datensätzen werden digitale Zwillinge immer präziser bei der Vorhersage individueller Behandlungsverläufe.
Herstellungsprozess Digitale Zwillinge
Über die Patientenversorgung hinaus modellieren digitale Zwillinge Fertigungsprozesse. Durch virtuelle Produktionssimulationen werden optimale Prozessparameter ermittelt, Ertragsergebnisse vorhergesagt und Prozessänderungen getestet, ohne dass tatsächliches Patientenmaterial verbraucht wird.
Diese Fähigkeit erweist sich als besonders wertvoll beim Technologietransfer - wenn Prozesse zwischen Entwicklungs- und kommerziellen Produktionsanlagen verschoben oder von kleinen auf große Produktionsmengen skaliert werden.
Innovation bei klinischen Prüfungen durch digitale Technologien
Digitale Technologien verändern die Art und Weise, wie klinische Studien konzipiert, durchgeführt und überwacht werden - besonders wichtig angesichts der begrenzten Patientenpopulationen für viele CGT-Indikationen.
Dezentrale Versuchskomponenten
Während für die Verabreichung von CGT spezielle Einrichtungen erforderlich sind, ermöglichen digitale Tools die Fernüberwachung von Patienten, virtuelle Konsultationen und gegebenenfalls die Probenentnahme zu Hause.
Mit tragbaren Geräten werden Sicherheitsparameter kontinuierlich und nicht nur bei einzelnen Klinikbesuchen erfasst. Die von den Patienten gemeldeten Ergebnisse fließen über mobile Anwendungen direkt in die Studiendatenbanken ein. Telemedizinische Plattformen ermöglichen häufige Kontrollbesuche ohne Reisestrapazen.
Datenintegration in der realen Welt
Die Amerikanische Gesellschaft für Gen- und Zelltherapie hat kürzlich eine Stellungnahme zur Unterstützung der Health Level Seven Fast Healthcare Interoperability Resources (HL7 FHIR) Standards für die Integration von Daten aus der Praxis eingereicht.
Daten aus der realen Welt, die aus elektronischen Gesundheitsakten, Versicherungsansprüchen und Patientenregistern erfasst werden, ergänzen die herkömmlichen Informationen aus klinischen Studien und bieten Einblicke in die langfristige Sicherheit, die Wirksamkeit in breiteren Bevölkerungsgruppen und vergleichbare Behandlungsergebnisse.
Die FDA prüft derzeit Rahmenbedingungen für die Einbeziehung von Erkenntnissen aus der Praxis in die Entscheidungsfindung der Behörden, insbesondere bei der Sicherheitsüberwachung nach der Zulassung und bei Überlegungen zur Erweiterung der Kennzeichnung.
Adaptive Versuchspläne
Digitale Datenplattformen ermöglichen adaptive Studiendesigns, die Protokolle auf der Grundlage der sich ansammelnden Erkenntnisse ändern. Bei Indikationen für seltene Krankheiten mit begrenzten Patientenpopulationen maximieren adaptive Ansätze den Informationsgewinn und minimieren gleichzeitig die Belastung der Patienten durch unwirksame Behandlungen.
In Studien der frühen Phase werden zunehmend die Ziele der Phasen 1 und 2 kombiniert, wobei der Schwerpunkt gleichzeitig auf der Sicherheit und der vorläufigen Wirksamkeit liegt. Dieser gestraffte Ansatz ist wissenschaftlich gerechtfertigt und angesichts des dringenden ungedeckten Bedarfs ethisch angemessen.
Regulatorische Erwägungen und Compliance-Rahmenwerke
Die digitale Transformation muss mit den sich entwickelnden regulatorischen Erwartungen in Einklang gebracht werden. Die FDA hat Leitlinien für fortschrittliche Fertigungstechnologien, künstliche Intelligenz in Medizinprodukten und digitale Gesundheitstechnologien in klinischen Studien herausgegeben.
Fortgeschrittene Fertigungstechnologien Bezeichnung
Die FDA hat im Dezember 2024 die endgültigen Leitlinien für das Programm zur Ausweisung fortschrittlicher Fertigungstechnologien veröffentlicht. In diesem Rahmen können Hersteller die Ausweisung spezifischer Technologien beantragen, die das Potenzial haben, die Produktqualität zu verbessern, Herstellungsrisiken zu verringern oder Arzneimittelengpässe zu beheben.
Ausgewiesene Technologien erhalten ein verstärktes Engagement der FDA, einschließlich Sitzungen zur Erörterung von Entwicklungsplänen, Herstellungsbewertungen und Regulierungspfaden. Diese proaktive Zusammenarbeit hilft Unternehmen, neue Technologien zu implementieren und gleichzeitig die Vorschriften einzuhalten.
Datenintegrität und Systemvalidierung
Digitale Systeme müssen strengen Anforderungen an die Datenintegrität genügen. Elektronische Aufzeichnungen benötigen Prüfpfade, die die Erstellung, Änderung und Löschung von Daten dokumentieren. Der Systemzugang erfordert rollenbasierte Kontrollen und regelmäßige Überprüfungen.
Die Validierung von Computersystemen zeigt, dass digitale Plattformen durchweg wie vorgesehen funktionieren. Validierungsprotokolle dokumentieren die Systemanforderungen, Testverfahren und die fortlaufende Überwachung und liefern so den Nachweis, dass die Systeme während ihres gesamten Lebenszyklus die Datenintegrität aufrechterhalten.
Aufsicht über KI und maschinelles Lernen
In dem Maße, wie KI-Technologien in die Entwicklung und Herstellung von CGT eingebettet werden, passen sich die rechtlichen Rahmenbedingungen an. Die FDA erkennt an, dass KI/ML-Systeme “komplexe und dynamische Prozesse” beinhalten, die andere Aufsichtsansätze als herkömmliche Software erfordern.
Zu den wichtigsten Aspekten gehören die Transparenz der Algorithmen, die Repräsentativität der Trainingsdaten, die Überwachung der Leistung während des Einsatzes und Verfahren zur Änderungskontrolle, wenn die Modelle auf der Grundlage neuer Daten aktualisiert werden.
Überwindung von Umsetzungshindernissen
Trotz eindeutiger Vorteile ist die digitale Transformation mit Hindernissen verbunden. Das Verständnis allgemeiner Hindernisse hilft Unternehmen bei der Entwicklung von Abhilfestrategien.
Kulturelle und organisatorische Widerstände
Die Umstellung von papiergestützten Arbeitsabläufen auf digitale Systeme erfordert einen kulturellen Wandel. Mitarbeiter, die an traditionelle Prozesse gewöhnt sind, können sich neuen Ansätzen widersetzen - vor allem, wenn die Schulung unzureichend ist oder die Vorteile nicht klar kommuniziert werden.
Bei erfolgreichen Implementierungen steht das Änderungsmanagement im Vordergrund:
- Einbeziehung der Endnutzer in die Auswahl der Technologie und die Gestaltung der Arbeitsabläufe
- Umfassende Schulung mit praktischen Übungsmöglichkeiten
- Identifizierung und Befähigung von Digital Champions in jedem Funktionsbereich
- Erste Erfolge feiern und Erfolgsgeschichten weit verbreiten
- Transparent auf Bedenken eingehen und Umsetzungen auf der Grundlage von Rückmeldungen anpassen
Komplexität der Systemintegration
CGT-Organisationen betreiben mehrere spezialisierte Systeme - Produktionsausführungssysteme, Laborinformationsmanagementsysteme, Unternehmensressourcenplanungsplattformen, Verwaltungssysteme für klinische Studien und vieles mehr.
Die Schaffung eines nahtlosen Datenflusses zwischen diesen Systemen erfordert eine sorgfältige Integrationsarchitektur. Anwendungsprogrammierschnittstellen ermöglichen die Kommunikation von System zu System, aber Integrationsprojekte erfordern erhebliche technische Ressourcen und Tests.
Viele Unternehmen verfolgen einen stufenweisen Ansatz, d. h. sie priorisieren zunächst die Integrationen mit dem höchsten Wert, anstatt sofort eine umfassende Verbindung zu versuchen.
Ressourcenbeschränkungen und ROI-Ungewissheit
Die digitale Transformation erfordert Vorabinvestitionen in Software, Infrastruktur, Beratungsdienste und Personalzeit. Bei kleineren Unternehmen oder solchen, die Therapien für extrem seltene Krankheiten entwickeln, können Ressourcenbeschränkungen die Einführung verzögern oder verhindern.
Der Aufbau klarer Geschäftsszenarien hilft, die Finanzierung zu sichern. Die Quantifizierung der erwarteten Vorteile - reduzierte Zykluszeiten, geringere Fehlerquoten, verbesserte Erträge, schnellere Einreichung von Anträgen bei den Behörden - führt zu greifbaren ROI-Prognosen, die Investitionen rechtfertigen.
Cloud-basierte Software-as-a-Service-Modelle reduzieren die anfänglichen Kapitalanforderungen im Vergleich zu On-Premise-Systemen und machen digitale Tools auch für Unternehmen mit begrenzten Budgets zugänglich.
| Bereich Herausforderung | Häufige Hindernisse | Strategien zur Schadensbegrenzung |
|---|---|---|
| Auswahl der Technologie | Überwältigende Anbieterlandschaft, unklare Funktionsdifferenzierung | Anforderungen zuerst definieren, Pilotprojekt vor vollem Einsatz, Referenzen von Kollegen einholen |
| Migration von Daten | Probleme mit der Datenqualität, Formatinkompatibilitäten | Daten proaktiv bereinigen, Migrationsvalidierungsprotokolle erstellen, stufenweises Vorgehen akzeptieren |
| Einhaltung von Vorschriften | Ungewissheit über Validierungsanforderungen, Bedenken hinsichtlich der Prüfungsbereitschaft | Frühzeitige Einbindung von Qualität/Rechtsvorschriften, Nutzung von Validierungspaketen der Anbieter, gründliche Dokumentation |
| Ausbildung des Personals | Zeitliche Beschränkungen, unterschiedliche technische Fertigkeiten | Rollenbasierte Schulungspfade, Super-User-Modell, laufende Support-Ressourcen |
| Lieferanten-Management | Beziehungen zu mehreren Anbietern, Abhängigkeiten bei der Integration | Priorisierung von Plattformen mit offenen APIs, Einführung einer klaren Governance, Pflege von Anbieter-Scorecards |
Globale Zugänglichkeit und gesundheitliche Chancengleichheit
Die digitale Transformation muss die Herausforderungen der globalen Zugänglichkeit berücksichtigen. Die Umsetzung von Zell- und Gentherapien in Ländern mit niedrigem und mittlerem Einkommen stößt auf erhebliche Hindernisse.
Zwischen 1991 und 2008 wurden nur etwa 2% der weltweit 274.000 klinischen Studien in Afrika durchgeführt, obwohl der Kontinent eine erhebliche Krankheitslast trägt. Begrenzte Regulierungskapazitäten, Infrastrukturlücken und Ressourcenbeschränkungen behindern den Zugang zu neuartigen Therapien.
Digitale Technologien bieten Teillösungen:
- Telemedizinische Plattformen ermöglichen Facharztkonsultationen aus der Ferne ohne teure Reisen
- Cloud-basierte Regulierungssysteme verringern die Anforderungen an die lokale Infrastruktur
- Gemeinsame Produktionsnetzwerke könnten mehrere Regionen effizient bedienen
- Digitale Schulungsprogramme bauen lokale Fähigkeiten auf, ohne dass Experten vor Ort reisen müssen
Mit Technologie allein lassen sich jedoch grundlegende Ungleichheiten beim Zugang zur Gesundheitsversorgung, bei den Finanzierungsmechanismen und den industriellen Kapazitäten nicht beseitigen. Die digitale Transformation sollte umfassendere Bemühungen um die weltweite Demokratisierung des Zugangs zu neuartigen Therapien ergänzen - und nicht ersetzen.
Zukünftige Richtungen und aufkommende Technologien
Die digitale Innovation in der CGT beschleunigt sich weiter. Mehrere neue Technologien sind besonders vielversprechend.
Blockchain für die Überprüfung der Lieferkette
Die Blockchain-Distributed-Ledger-Technologie erstellt unveränderliche Aufzeichnungen über die Handhabung des Produkts, die Lagerbedingungen und die Übertragung der Verwahrung. Für autologe Therapien, die eine absolute Sicherheit der Identitätskette erfordern, bietet Blockchain eine kryptografisch verifizierte Rückverfolgbarkeit.
Erste Implementierungen zeigen die Machbarkeit, doch die breite Einführung muss noch genormt und in bestehende Systeme integriert werden.
Erweiterte Analytik und vorausschauende Fertigung
Modelle des maschinellen Lernens, die auf historischen Fertigungsdaten trainiert wurden, können Chargenergebnisse vorhersagen, Prozessabweichungen erkennen, bevor sie sich auf die Qualität auswirken, und Parameteranpassungen zur Optimierung des Ertrags empfehlen.
Mit der Zunahme von Produktionsdaten werden die Vorhersagefähigkeiten verbessert - und ermöglichen möglicherweise eine "Lights-Out"-Fertigung mit minimalen menschlichen Eingriffen für Routineproduktionsschritte.
Synthetische Biologie und Computergestaltung
Computergestützte Werkzeuge beschleunigen die Entwicklung von Zelltherapien. Anstelle von empirischen Versuchen und Irrtümern werden in der synthetischen Biologie Modelle verwendet, um genetische Schaltkreise zu entwerfen, das Zellverhalten vorherzusagen und therapeutische Konstrukte in silico zu optimieren, bevor sie physikalisch getestet werden.
Diese Fähigkeit zur rechnergestützten Entwicklung ergänzt die digitalen Zwillinge - gemeinsam schaffen sie umfassende virtuelle Umgebungen für die Therapieentwicklung und -optimierung.
Praktischer Fahrplan für die Umsetzung
Unternehmen, die mit der digitalen Transformation beginnen, sollten einen strukturierten Ansatz verfolgen und nicht ad hoc Technologien einführen.
Schritt 1: Bewertung des aktuellen Zustands
Dokumentieren Sie bestehende Prozesse, Systeme und Datenflüsse. Identifizieren Sie Schwachstellen, Ineffizienzen und Compliance-Risiken. Bewertung des digitalen Reifegrads in den Bereichen Herstellung, Qualität, klinische und kommerzielle Funktionen.
Schritt 2: Definition der strategischen Vision
Legen Sie klare Ziele fest, die auf die Prioritäten des Unternehmens abgestimmt sind. Welche spezifischen Ergebnisse soll die digitale Transformation erzielen? Kürzere Markteinführungszeiten? Verbesserte Produktqualität? Bessere Patientenergebnisse? Niedrigere Produktionskosten?
Priorisierung der Anwendungsfälle auf der Grundlage der erwarteten Auswirkungen und der Durchführbarkeit der Implementierung.
Schritt 3: Geeignete Technologien auswählen
Bewerten Sie Plattformen anhand der definierten Anforderungen. Berücksichtigen Sie Integrationsfunktionen, die Stabilität des Anbieters, die Einhaltung gesetzlicher Vorschriften, Skalierbarkeit und die Gesamtbetriebskosten.
Vermeiden Sie technologieorientierte Ansätze, bei denen Werkzeuge ausgewählt werden, bevor der Bedarf bekannt ist.
Schritt 4: Durchführung von gezielten Piloten
Testen ausgewählter Technologien in kontrollierten Bereichen vor der unternehmensweiten Einführung. Pilotprojekte validieren die erwarteten Vorteile, identifizieren die Herausforderungen bei der Implementierung und schaffen Vertrauen im Unternehmen.
Dokumentation der Erfahrungen und Verfeinerung der Ansätze vor der Ausweitung.
Schritt 5: Erfolgreiche Initiativen skalieren
Ausweitung bewährter Pilotprojekte auf weitere Standorte, Produkte oder Funktionen. Investieren Sie in Schulungen, Änderungsmanagement und die laufende Support-Infrastruktur.
Schaffung eines Governance-Rahmens, der eine konsistente Bereitstellung gewährleistet und unautorisierte Systemänderungen verhindert.
Schritt 6: Kontinuierliche Optimierung
Überwachen Sie Leistungskennzahlen, sammeln Sie Nutzerfeedback, und verbessern Sie Prozesse iterativ. Die digitale Transformation ist kein einmaliges Projekt - sie ist eine fortlaufende Fähigkeit, die kontinuierliche Aufmerksamkeit erfordert.
Bleiben Sie über Branchenverbände, Konferenzen und Netzwerke auf dem Laufenden, was neue Technologien und sich ändernde behördliche Auflagen betrifft.
| Durchführungsphase | Typische Dauer | Wichtigste Ergebnisse | Erfolgsmetriken |
|---|---|---|---|
| Bewertung | 1-2 Monate | Dokumentation des Ist-Zustands, Gap-Analyse, Reifegrad-Bewertung | Umfassendes Verständnis der grundlegenden Fähigkeiten |
| Strategieentwicklung | 1-2 Monate | Visionserklärung, priorisierte Anwendungsfälle, Roadmap, Business Case | Anpassung an die Bedürfnisse der Exekutive und Genehmigung der Finanzierung |
| Auswahl der Technologie | 2-3 Monate | Anforderungsdokument, Lieferantenbewertungen, Auswahlentscheidung | Auf die Anforderungen abgestimmte Plattformentscheidungen |
| Pilot-Ausführung | 3-6 Monate | Konfiguriertes System, geschulte Benutzer, Pilotergebnisse, gewonnene Erfahrungen | Validierte Vorteile, verfeinerter Implementierungsansatz |
| Skalierung des Einsatzes | 6-18 Monate | Unternehmenseinführung, erweiterte Schulung, Abschluss der Integration | Annahmeziele, Leistungsverbesserungen |
| Kontinuierliche Optimierung | Laufend | Leistungsübersichten, regelmäßige Überprüfungen, Verbesserungsrückstand | Nachhaltiger Nutzen, Nutzerzufriedenheit, wachsende Leistungsfähigkeit |
Aufbau zuverlässiger digitaler Grundlagen für die Zell- und Gentherapie
Die Arbeit in der Zell- und Gentherapie hängt von genauen Daten, nachvollziehbaren Prozessen und Systemen ab, die sowohl die Forschung als auch die Produktion bewältigen können, ohne die Kontinuität zu unterbrechen. A-listware unterstützt Organisationen, indem es untersucht, wie Daten, Systeme und Arbeitsabläufe derzeit strukturiert sind, und sie dann neu organisiert, um die Konsistenz und Kontrolle zu verbessern.
Dazu gehört häufig, dass die Speicherung von und der Zugriff auf Informationen verbessert, manuelle Übergaben reduziert und sichergestellt wird, dass die Systeme das Wachstum unterstützen können, ohne dass Lücken zwischen den einzelnen Arbeitsschritten entstehen. Wenn Ihre derzeitige Struktur es erschwert, die Kontrolle zu behalten oder sicher zu skalieren, wenden Sie sich an A-listware um eine klare, praktische Vorstellung davon zu bekommen, wie es weitergehen soll.
Messung des Erfolgs der digitalen Transformation
Quantifizierbare Metriken zeigen den Wert der Transformation und dienen der laufenden Verbesserung.
Zu den Fertigungskennzahlen gehören die Verringerung der Zykluszeit, die Erfolgsquote von Chargen, die Häufigkeit von Abweichungen und die Zeit bis zur Freigabe. Führende Unternehmen berichten von 20-40% Verbesserungen in diesen Bereichen nach der Digitalisierung.
Anhand von Qualitätskennzahlen lassen sich Fehlerquoten, Untersuchungszeiträume, Prüfungsergebnisse und Inspektionsresultate verfolgen. Elektronische Systeme reduzieren Dokumentationsfehler in der Regel um 60-80% im Vergleich zu Papierverfahren.
Klinische Metriken messen die Patientenrekrutierungsraten, die Häufigkeit von Protokollabweichungen, die Datenqualität und die Effizienz der Überwachung. Digitale Tools können die Rekrutierungszeiten um 30% oder mehr verkürzen.
Zu den Finanzkennzahlen gehören Kosten pro Charge, Lagerhaltungskosten, Arbeitsproduktivität und Rentabilität der digitalen Investition. Umfassende Umstellungen erzielen in der Regel innerhalb von 18-36 Monaten einen positiven ROI.
Häufig gestellte Fragen
- Was sind die größten Herausforderungen bei der digitalen Transformation der Zell- und Gentherapieherstellung?
Zu den wichtigsten Herausforderungen gehören die Komplexität der Systemintegration über mehrere spezialisierte Plattformen hinweg, der kulturelle Widerstand von Mitarbeitern, die an papierbasierte Arbeitsabläufe gewöhnt sind, Ressourcenbeschränkungen, die die Vorabinvestitionen begrenzen, Unsicherheiten bei der Einhaltung von Vorschriften im Zusammenhang mit neuen Technologien und die Datenmigration von Altsystemen. Unternehmen überwinden diese Hindernisse durch schrittweise Implementierungen, ein starkes Änderungsmanagement, eine klare ROI-Darstellung und eine frühzeitige Einbeziehung der Behörden.
- Wie verbessern digitale Zwillinge die Ergebnisse der CAR-T-Zelltherapie?
Digitale Zwillinge erstellen patientenspezifische virtuelle Modelle, indem sie genomische Daten, Tumoreigenschaften, Immunprofile, Bildgebungsergebnisse und die Krankengeschichte integrieren. Diese multiskaligen Simulationen sagen das individuelle Ansprechen auf die Behandlung voraus, optimieren die Dosierungsstrategien, identifizieren die Patienten, die am ehesten davon profitieren, und ermöglichen die frühzeitige Erkennung von Rückfall-Signalen. Algorithmen des maschinellen Lernens verbessern die Vorhersagegenauigkeit bei wachsenden Datensätzen, wodurch digitale Zwillinge für die Personalisierung von Therapieansätzen immer wertvoller werden.
- Welche rechtlichen Leitlinien gibt es für fortschrittliche Fertigungstechnologien in der CGT?
Die FDA hat im Dezember 2024 einen Leitfaden zur Einführung des Programms für fortschrittliche Fertigungstechnologien (Advanced Manufacturing Technologies Designation Program) fertiggestellt. In diesem Rahmen können Hersteller die Ausweisung von Technologien beantragen, die die Qualität verbessern, Risiken verringern oder Engpässe beseitigen. Für ausgewiesene Technologien gibt es ein verstärktes Engagement der FDA, einschließlich Entwicklungssitzungen und Diskussionen über den Regulierungspfad. Weitere Leitlinien befassen sich mit KI/ML in Medizinprodukten, digitalen Gesundheitstechnologien in Studien und Datenintegritätsanforderungen für elektronische Systeme.
- Wie lange dauert die digitale Transformation bei Zell- und Gentherapieunternehmen in der Regel?
Der Zeitrahmen hängt vom Umfang und der Bereitschaft der Organisation ab. Die anfängliche Bewertung und Strategieentwicklung dauert 2-4 Monate. Die Technologieauswahl dauert 2-3 Monate. Pilotprojekte dauern 3-6 Monate. Die Einführung auf Unternehmensebene dauert 6-18 Monate für eine umfassende Umgestaltung. Unternehmen sollten dies jedoch als kontinuierliche Entwicklung und nicht als begrenzte Projekte betrachten - die laufende Optimierung wird unbegrenzt fortgesetzt, da sich die Technologien und Anforderungen weiterentwickeln.
- Können sich kleinere Biotech-Unternehmen Initiativen zur digitalen Transformation leisten?
Ja, aber die Ansätze unterscheiden sich von denen großer Pharmaunternehmen. Cloud-basierte Software-as-a-Service-Plattformen verringern den Kapitalbedarf im Vergleich zu Vor-Ort-Systemen. Gezielte Implementierungen, die auf die Anwendungsfälle mit dem höchsten Wert abzielen, bieten Vorteile ohne umfassende Unternehmensimplementierungen. Auftragsentwicklungs- und -fertigungsunternehmen bieten zunehmend digitale Dienstleistungen an, die es kleinen Unternehmen ermöglichen, auf fortschrittliche Funktionen zuzugreifen, ohne eine interne Infrastruktur aufzubauen. Stufenweise Ansätze verteilen die Kosten über die Zeit und liefern gleichzeitig einen zusätzlichen Wert.
- Wie verbessert die Digitalisierung das Lieferkettenmanagement für autologe Therapien?
Digitale Plattformen für die Lieferkette integrieren die Planung der Abholstellen, die Verfolgung der Logistik, die Aktualisierung des Produktionsstatus und die Koordination der Behandlungszentren in einheitliche Systeme. Die Echtzeittransparenz ermöglicht ein proaktives Ausnahmemanagement anstelle einer reaktiven Brandbekämpfung. Identitätsketten-Systeme mit biometrischer Verifizierung, RFID-Etiketten und Barcode-Scanning gewährleisten die Rückverfolgbarkeit der Produkte von der Apherese bis zur Infusion. Temperaturüberwachung, Routenoptimierung und automatische Dokumentation reduzieren Fehler und beschleunigen die Zeitspanne von der Vene zur Vene um 15-30%.
- Welche Rolle spielen Daten aus der Praxis bei der Entwicklung von Zell- und Gentherapien?
Daten aus der realen Welt, die aus elektronischen Gesundheitsakten, Anspruchsdatenbanken und Patientenregistern stammen, bieten Einblicke in die langfristige Sicherheit, die Wirksamkeit in verschiedenen Bevölkerungsgruppen und vergleichende Behandlungsergebnisse außerhalb kontrollierter Studien. Die FDA arbeitet an der Entwicklung von Rahmenwerken zur Einbeziehung von Real-World-Evidenzen in Zulassungsentscheidungen, insbesondere für die Sicherheitsüberwachung nach der Zulassung, für die Ausweitung der Kennzeichnung und für seltene Krankheiten, bei denen herkömmliche Studien Probleme bei der Rekrutierung haben. Standardisierte Datenformate wie HL7 FHIR ermöglichen eine effiziente Integration von Real-World-Daten in Entwicklungsprogramme.
Schlussfolgerung
Die digitale Transformation bedeutet mehr als nur die Einführung von Technologien - sie bedeutet eine grundlegende Neukonzeption der Art und Weise, wie Zell- und Gentherapien entwickelt, hergestellt und an Patienten geliefert werden.
Von KI-gestützter Behandlungsvorhersage bis hin zu automatisierten Fertigungsplattformen - digitale Tools lösen kritische Herausforderungen, die die Skalierbarkeit und Zugänglichkeit von CGT einschränken. Unternehmen, die diese Technologien einsetzen, berichten von kürzeren Entwicklungszeiten, verbesserter Produktqualität, geringeren Kosten und besseren Patientenergebnissen.
Doch Technologie allein ist keine Garantie für Erfolg. Eine wirksame Umgestaltung erfordert eine strategische Vision, eine funktionsübergreifende Zusammenarbeit, eine Anpassung der Vorschriften, ein Änderungsmanagement und eine kontinuierliche Optimierung. Unternehmen müssen ein Gleichgewicht zwischen Innovation und Einhaltung von Vorschriften, Geschwindigkeit und Qualität sowie Automatisierung und menschlicher Kontrolle finden.
Die Unterstützung der FDA für fortschrittliche Fertigungstechnologien durch Ausweisungsprogramme und verstärktes Engagement schafft ein günstiges regulatorisches Umfeld für Innovationen. In dem Maße, wie die digitalen Möglichkeiten reifen und die Akzeptanz zunimmt, wird die Zell- und Gentherapie zunehmend ihr Versprechen einlösen, bisher unbehandelbare Krankheiten zu heilen.
Für CGT-Organisationen ist es jetzt an der Zeit, den digitalen Reifegrad zu bewerten, hochwertige Möglichkeiten zu identifizieren und mit der Transformation zu beginnen. Die Wettbewerbsvorteile - und der Nutzen für die Patienten - machen die digitale Transformation nicht nur nützlich, sondern unerlässlich.
Sind Sie bereit, die digitale Transformation in Ihrem Unternehmen voranzutreiben? Beginnen Sie damit, die aktuellen Fähigkeiten im Vergleich zu Branchen-Benchmarks zu bewerten, Schmerzpunkte mit messbaren Auswirkungen auf das Geschäft zu identifizieren und Initiativen zu priorisieren, die schnelle Erfolge bringen, während Sie auf umfassende Veränderungen hinarbeiten.


