Résumé rapide : La transformation numérique pour le biotraitement combine l'IA, les jumeaux numériques, l'analyse des données en temps réel et la modélisation hybride pour révolutionner la bioproduction. Selon les études de marché (par exemple, Fortune Business Insights), la taille du marché mondial de l'intelligence artificielle devrait passer de $294,16 milliards en 2025 à $1771,62 milliards d'ici 2032, affichant un TCAC de 29,2%. Ces technologies permettent aux fabricants d'optimiser les processus de culture cellulaire, d'accélérer la libération des lots, de réduire les coûts de développement et de maintenir la conformité réglementaire dans un environnement de production de plus en plus complexe.
L'industrie biopharmaceutique est à la croisée des chemins. Avec des taux d'attrition des candidats-médicaments de 96% et des coûts de développement moyens de plus de $3 milliards, les fabricants ne peuvent pas se permettre de s'appuyer sur des approches traditionnelles. La transformation numérique n'est pas un simple mot à la mode - elle est en train de devenir le système d'exploitation fondamental du biotraitement moderne.
Mais voilà : la mise en œuvre de solutions numériques dans le secteur des bioprocédés n'est pas aussi simple que l'installation d'un nouveau logiciel. Les environnements de fabrication génèrent des quantités massives de données, mais la plupart des organisations ont du mal à transformer ces informations en informations exploitables.
Ce guide explique précisément comment les technologies numériques remodèlent les bioprocédés, quels sont les outils qui donnent réellement des résultats et ce que les fabricants doivent savoir pour rester compétitifs.
Pourquoi la transformation numérique est importante aujourd'hui
Le paysage des bioprocédés a radicalement changé. L'adoption de l'IA générative dans le secteur biopharmaceutique a atteint 54% d'ici 2025, selon les tendances de l'industrie des sciences de la vie. Mais l'adoption seule ne garantit pas le succès.
La fabrication traditionnelle repose sur la collecte manuelle de données, l'échantillonnage périodique et l'analyse rétrospective des lots. Cette approche pose plusieurs problèmes :
- Les écarts entre les lots ne sont pas détectés jusqu'à ce qu'il soit trop tard pour les corriger.
- L'optimisation des processus se fait lentement par essais et erreurs
- Les échecs de mise à l'échelle font perdre du temps et des ressources
- La documentation réglementaire devient un goulot d'étranglement
En réalité, ces limitations ont un impact direct sur les résultats. Les processus de purification des anticorps monoclonaux permettent généralement de récupérer 70% de produit avec une pureté supérieure à 95%, selon une étude publiée dans la revue Biotechnology and Bioengineering. Pourtant, de nombreux fabricants laissent un rendement important sur la table parce qu'ils ne peuvent pas identifier les possibilités d'optimisation en temps réel.
Les technologies de base à l'origine de la transformation
Plusieurs technologies numériques font leurs preuves dans les environnements de biotraitement. Chacune d'entre elles permet de relever des défis spécifiques dans le processus de fabrication.
Jumeaux numériques et modélisation virtuelle
Les jumeaux numériques créent des représentations virtuelles de systèmes physiques de biotraitement. Ces modèles simulent la manière dont les modifications des paramètres du processus affectent les résultats avant de les mettre en œuvre dans la production.
Une étude publiée dans l'International Journal of Pharmaceutics montre comment les jumeaux numériques réduisent les risques depuis la découverte des médicaments jusqu'à la fabrication en continu. La technologie permet aux fabricants de tester virtuellement des scénarios, en identifiant les problèmes potentiels avant qu'ils n'aient un impact sur les lots de production réels.
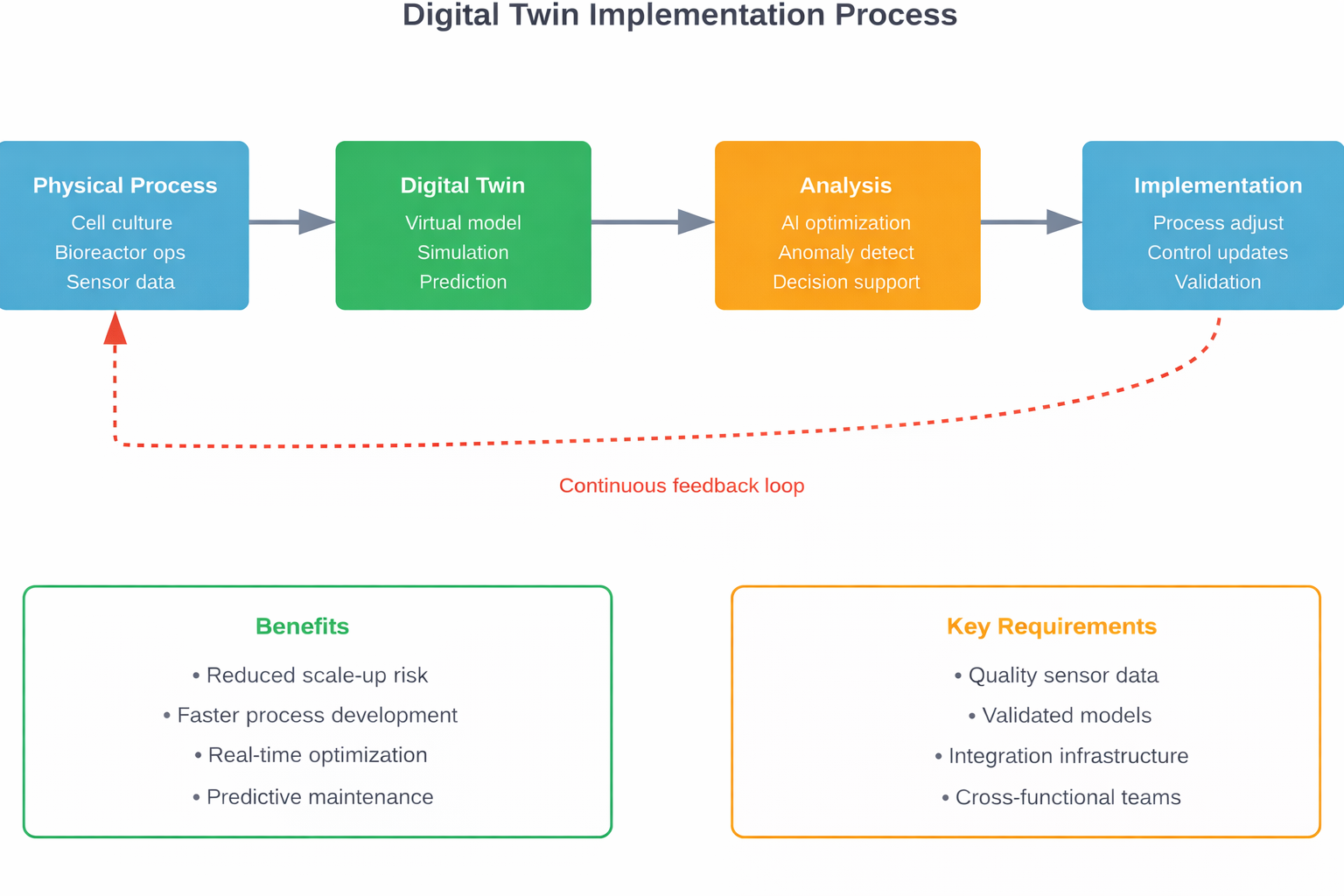
Les modèles de cellules CHO les plus avancés comprennent désormais 3 597 gènes, 11 004 réactions et 7 377 métabolites, selon une étude publiée dans le Computational and Structural Biotechnology Journal. Ce niveau de détail permet des prédictions métaboliques précises qui n'étaient pas possibles avec des modèles plus simples.
Analyse des données en temps réel et PAT
La technologie analytique des procédés permet un contrôle continu tout au long de la fabrication. Au lieu d'attendre les résultats des laboratoires hors ligne, les systèmes PAT fournissent un retour d'information immédiat sur les attributs de qualité critiques.
Les bioprocédés définis par les données vont encore plus loin en créant un flux de données transparent entre les systèmes. Cela permet à l'IA d'optimiser en permanence les opérations tout en prenant automatiquement des décisions analytiques.
Un fabricant mondial de vaccins a appliqué ces principes pour améliorer le rendement sur la base d'un historique de fabrication d'environ 10 ans couvrant des milliers de paramètres. Le système génère automatiquement des rapports en temps réel, ce qui accélère la libération des lots en permettant un examen par exception plutôt que des vérifications manuelles exhaustives.
Approches de modélisation hybrides
Les modèles hybrides combinent la compréhension mécaniste et l'apprentissage automatique. La composante mécaniste saisit les principes biologiques et chimiques connus. L'apprentissage automatique comble les lacunes là où la compréhension fondamentale reste incomplète.
Cette approche s'avère particulièrement précieuse pour les bioprocédés complexes où les modèles mécanistes purs deviennent difficiles à manier et où les modèles ML purs manquent d'interprétabilité. Les modèles hybrides permettent d'équilibrer efficacement ces deux besoins.
Mise en œuvre de solutions numériques
Le choix de la technologie importe moins que la stratégie de mise en œuvre. De nombreuses initiatives de transformation numérique échouent non pas à cause de mauvais outils, mais en raison d'une planification et d'une gestion du changement inadéquates.
Commencer par les principes de la qualité dès la conception
La qualité dès la conception (Quality by Design) constitue la base du bioprocessus numérique. La QbD identifie les paramètres critiques du processus et les attributs de qualité avant de sélectionner les outils numériques pour les surveiller et les contrôler.
La réglementation de la FDA sur les bonnes pratiques de fabrication met l'accent sur la compréhension et le contrôle des processus. Les technologies numériques soutiennent la conformité en fournissant une documentation continue et une surveillance des processus en temps réel.
| Élément QbD | Soutien à la technologie numérique | Bénéfice principal |
|---|---|---|
| Définition de l'espace de conception | Jumeaux numériques, logiciel DoE | Une optimisation plus rapide |
| Surveillance des paramètres critiques | Capteurs PAT, analyse en temps réel | Détection immédiate des écarts |
| Compréhension du processus | Modèles hybrides, analyse de l'IA | Approfondissement des mécanismes |
| Stratégie de contrôle | Systèmes de contrôle automatisés | Qualité constante |
| Amélioration continue | Lacs de données, algorithmes ML | Optimisation continue |
Construire d'abord l'infrastructure des données
Les analyses sophistiquées nécessitent des données de qualité. Mais attendez, cela signifie que les investissements dans l'infrastructure précèdent le développement des algorithmes.
Les principaux éléments de l'infrastructure sont les suivants
- Formats de données normalisés entre les instruments et les systèmes
- Stockage sécurisé des données avec des politiques de conservation appropriées
- Plateformes d'intégration reliant des systèmes de fabrication disparates
- Contrôle des versions pour les paramètres et les modèles de processus
La recherche dans la revue MAbs met l'accent sur les plateformes numériques unifiées pour l'analyse des données et la gestion des flux de travail. Les systèmes fragmentés créent des silos de données qui nuisent à l'analyse avancée.
Aborder les questions réglementaires de manière proactive
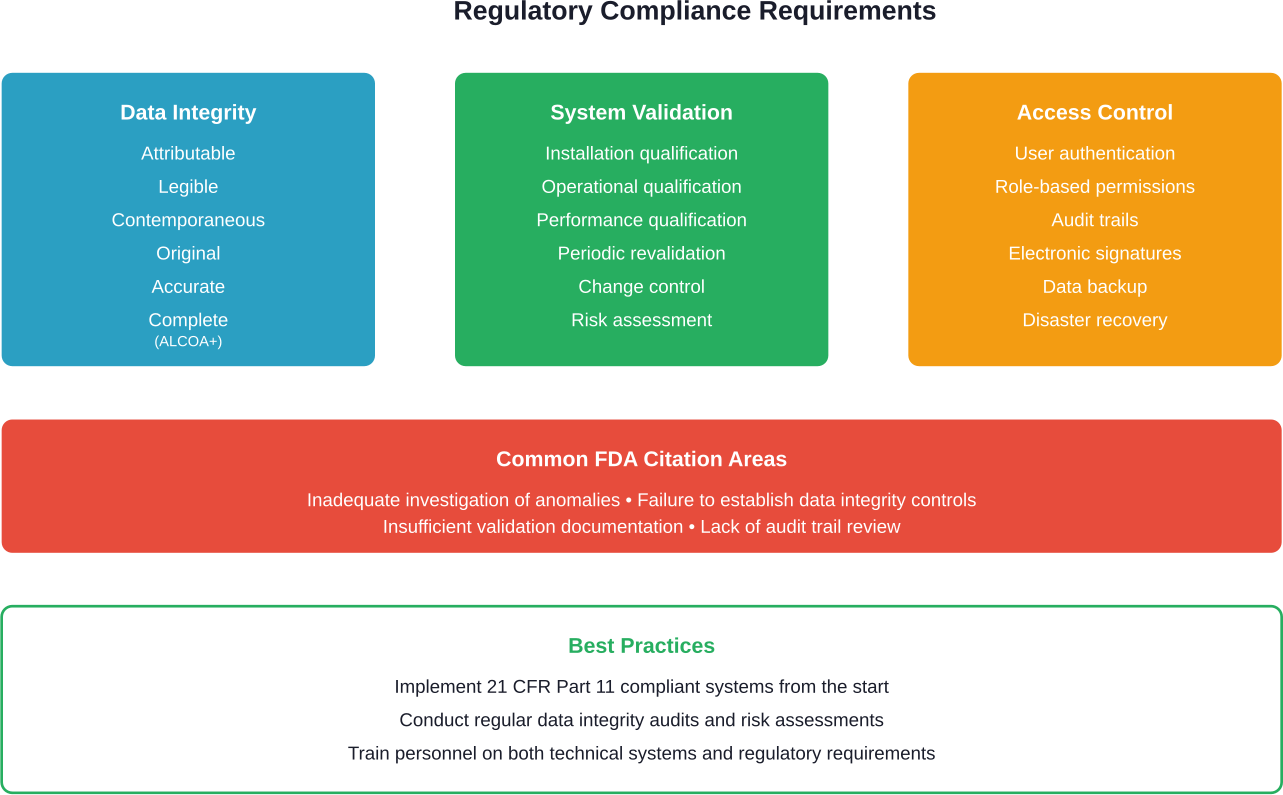
Les systèmes numériques doivent répondre aux exigences réglementaires en matière de fabrication de produits pharmaceutiques. Cela inclut les principes d'intégrité des données connus sous le nom d'ALCOA+ (Attribuable, Legible, Contemporaneous, Original, Accurate, plus complete, consistent, enduring, and available).
Les lettres d'avertissement de la FDA font souvent état de violations des CGMP liées à l'intégrité des données. Les systèmes numériques doivent être validés, avec des contrôles d'accès appropriés, des pistes d'audit et des procédures de gestion des changements.
Moderniser l'infrastructure des bioprocédés avec le soutien adéquat
Les entreprises de biotransformation sont souvent confrontées à des systèmes déconnectés, des logiciels hérités et des environnements de données complexes qui ralentissent la production et l'analyse. La transformation numérique se concentre sur la mise à niveau des plateformes de base, la connexion des systèmes de laboratoire et de fabrication, et l'amélioration de la façon dont les données opérationnelles circulent entre les équipes.
A-listware soutient les organisations qui ont besoin de moderniser leur pile technologique. Leurs ingénieurs aident à revoir l'infrastructure existante, à mettre à niveau les systèmes existants et à mettre en œuvre des logiciels évolutifs ou des environnements en nuage qui soutiennent mieux les flux de travail de production et de recherche.
Si vos systèmes de bioprocédés ont besoin d'une base numérique stable, faites appel à Logiciel de liste A pour aider à planifier et à mettre en œuvre la transition.
Fabrication continue et intensification des processus
La fabrication en continu représente un changement fondamental par rapport à la production par lots. Cette approche réduit l'encombrement des installations, améliore la cohérence et permet une assurance qualité en temps réel.
Mais il y a un hic : les processus continus génèrent une quantité exponentielle de données par rapport aux opérations par lots. Sans systèmes numériques pour gérer cette complexité, la charge opérationnelle devient écrasante.
La technologie analytique des procédés devient essentielle plutôt qu'optionnelle dans la fabrication en continu. La surveillance et le contrôle en temps réel permettent de maintenir les processus dans les limites des spécifications sans intervention manuelle.
Research in Biotechnology and Bioengineering note que la purification des anticorps monoclonaux vise généralement à obtenir moins de 100 ppm de protéines de la cellule hôte, moins de 10 ng par dose d'ADN de la cellule hôte et une pureté du produit supérieure à 95%. Les processus continus avec PAT intégré maintiennent ces spécifications de manière plus cohérente que les opérations par lots.
Applications de l'IA et de l'apprentissage automatique
L'intelligence artificielle ajoute des capacités de prédiction et d'optimisation aux bioprocédés. La technologie a dépassé le stade des projets pilotes pour entrer dans des environnements de production chez des fabricants de premier plan.
L'analyse prédictive pour l'optimisation des processus
Les algorithmes d'apprentissage automatique identifient dans les données historiques de fabrication des schémas qui échappent aux humains. Ces modèles révèlent les relations entre les paramètres du processus et les attributs de qualité du produit.
Les modèles prédictifs prévoient les résultats des lots sur la base d'indicateurs de processus précoces. Cela permet de prendre des mesures correctives avant que les problèmes de qualité ne se développent, ce qui réduit les échecs des lots et améliore le rendement.
Détection des anomalies et alertes en temps réel
Les systèmes d'IA surveillent en permanence les paramètres des processus et signalent les écarts par rapport aux plages de fonctionnement normales. Contrairement aux simples alertes de seuil, la détection d'anomalies basée sur l'intelligence artificielle tient compte des interactions complexes entre les paramètres et des dérives subtiles.
Cela s'avère particulièrement utile pour identifier les problèmes d'équipement avant qu'ils n'affectent la qualité du produit. La maintenance prédictive réduit les temps d'arrêt imprévus et prolonge la durée de vie des équipements.
| Application de l'IA | Complexité de la mise en œuvre | Calendrier type du retour sur investissement |
|---|---|---|
| Résultats prédictifs des lots | Moyen | 6-12 mois |
| Détection des anomalies en temps réel | Moyenne-élevée | 3-9 mois |
| Optimisation des processus | Haut | 12-24 mois |
| Libération automatisée des lots | Haut | 18-36 mois |
| Maintenance prédictive | Moyen | 6-18 mois |
Surmonter les difficultés de mise en œuvre
La transformation numérique se heurte à des obstacles prévisibles. S'attaquer à ces obstacles de manière proactive augmente les chances de réussite.
Qualité et disponibilité des données
De nombreuses organisations découvrent que leurs données historiques ne sont pas adaptées à l'analyse avancée. Les formats incohérents, les métadonnées manquantes et les lacunes dans les données limitent l'apprentissage des modèles.
Commencer par la collecte de données prospectives - avant même de mettre en œuvre des analyses avancées - permet de jeter les bases d'initiatives futures. Des données propres et bien organisées deviennent un atout qui s'apprécie au fil du temps.
Compétences et changement organisationnel
Les bioprocédés numériques nécessitent une collaboration interfonctionnelle entre les ingénieurs des procédés, les scientifiques des données, les professionnels de la qualité et les spécialistes des technologies de l'information. Ces groupes parlent souvent des langues différentes et ont des priorités différentes.
Les organisations qui réussissent créent des équipes intégrées ayant des objectifs communs. Les programmes de formation aident le personnel de fabrication traditionnel à acquérir des compétences en matière de données tout en enseignant aux scientifiques des données les principes fondamentaux du biotraitement.
Intégration avec les systèmes existants
La plupart des établissements utilisent un mélange d'équipements modernes et anciens. Les systèmes anciens peuvent manquer de connectivité numérique ou utiliser des formats de données propriétaires.
Les plateformes middleware comblent ces lacunes, en extrayant les données des systèmes existants et en les convertissant dans des formats standardisés. Bien qu'elle ne soit pas idéale, cette approche permet la transformation numérique sans remplacer prématurément les équipements fonctionnels.
Mesurer le succès et le retour sur investissement
Les initiatives numériques nécessitent des mesures de réussite claires. La justification financière reste importante, mais les organisations les plus performantes suivent également les améliorations opérationnelles et qualitatives.
Les principaux indicateurs de performance sont les suivants
- Amélioration du rendement des lots et réduction de la variabilité des processus
- Des délais de développement plus courts, du concept à la production commerciale
- Réduction des échecs de lots et des cycles d'investigation
- Amélioration de l'utilisation des équipements et réduction des temps d'arrêt
- Libération plus rapide des lots grâce à l'examen automatisé des données
Le coût moyen estimé pour le développement d'un nouveau médicament était d'environ $2,6 milliards (en dollars de 2013), mais une fois corrigé de l'inflation d'ici 2026, ce chiffre dépasse $3 milliards.
Orientations futures
Les bioprocédés numériques continuent d'évoluer rapidement. Plusieurs tendances émergentes méritent l'attention.
Les systèmes d'IA multimodale intègrent divers types de données : séquences génomiques, structures protéiques, paramètres de processus et données sur la qualité des produits. Cette approche holistique révèle des relations invisibles lors de l'analyse de types de données isolés.
L'informatique en périphérie rapproche l'analyse avancée de l'équipement de fabrication. Cela réduit le temps de latence pour un contrôle en temps réel, tout en répondant aux préoccupations en matière de sécurité des données liées à la connectivité en nuage.
La médecine personnalisée pose des défis uniques en matière de fabrication. Les outils numériques permettent de mettre en place des systèmes de production flexibles capables de fabriquer efficacement de petits lots de thérapies spécifiques aux patients.
Questions fréquemment posées
- Qu'est-ce que la transformation numérique dans le domaine des bioprocédés ?
La transformation numérique dans le domaine des bioprocédés fait référence à l'intégration de technologies avancées telles que l'IA, les jumeaux numériques, l'analyse en temps réel et les systèmes de contrôle automatisés dans les opérations de bioproduction. Cela permet une prise de décision basée sur les données, l'optimisation des processus et l'amélioration continue plutôt que de s'appuyer uniquement sur les approches manuelles traditionnelles et le contrôle de la qualité basé sur les lots.
- Comment les jumeaux numériques améliorent-ils le développement des bioprocédés ?
Les jumeaux numériques créent des modèles virtuels de systèmes de biotraitement qui simulent la façon dont les changements de paramètres affectent les résultats avant leur mise en œuvre. Cela permet de réduire les risques liés à la mise à l'échelle, d'accélérer le développement des processus et de permettre l'optimisation par le biais de l'expérimentation virtuelle. La recherche montre que les jumeaux numériques peuvent inclure des milliers de réactions métaboliques et d'éléments génétiques, fournissant des prédictions détaillées du comportement des cultures cellulaires.
- Que sont les bioprocédés définis par les données ?
Les bioprocédés définis par les données utilisent un flux de données en temps réel intégré dans les systèmes, l'IA optimisant en permanence les opérations et prenant des décisions analytiques. Au lieu de procéder à des échantillonnages manuels périodiques et à des analyses hors ligne, ces systèmes fournissent un retour d'information immédiat sur les performances du processus, ce qui permet de prendre plus rapidement des mesures correctives et d'automatiser la libération des lots par le biais d'un examen fondé sur les exceptions.
- Comment le PAT soutient-il le biotraitement numérique ?
La technologie analytique de processus permet une surveillance continue des paramètres de processus critiques et des attributs de qualité tout au long de la fabrication. La PAT génère des données en temps réel qui alimentent les jumeaux numériques, les algorithmes d'optimisation de l'IA et les systèmes de contrôle automatisés. Cela permet de détecter les écarts et de réagir immédiatement plutôt que de découvrir les problèmes uniquement lors des tests de fin de lot.
- Quelles sont les considérations réglementaires qui s'appliquent aux systèmes numériques de biotraitement ?
Les systèmes numériques doivent être conformes à la réglementation de la FDA sur les bonnes pratiques de fabrication, y compris les exigences en matière d'intégrité des données. Les systèmes doivent disposer d'une documentation de validation, de pistes d'audit, de contrôles d'accès et de capacités de signature électronique. La FDA insiste sur le fait que les outils numériques doivent améliorer la compréhension et le contrôle des processus tout en conservant des données attribuables, lisibles, contemporaines, originales et exactes.
- Quelles sont les compétences nécessaires à la mise en œuvre des bioprocédés numériques ?
Une mise en œuvre réussie nécessite des équipes interfonctionnelles combinant des connaissances en ingénierie des bioprocédés, une expertise en science des données, une compréhension des systèmes de qualité et des capacités en matière d'infrastructure informatique. Les organisations ont souvent besoin de programmes de formation pour développer la maîtrise des données parmi le personnel de fabrication traditionnel, tout en enseignant aux scientifiques des données les principes fondamentaux des bioprocédés et les exigences réglementaires.
- Quel retour sur investissement les organisations peuvent-elles attendre des initiatives de biotraitement numérique ?
Le retour sur investissement varie en fonction de l'application et de la qualité de la mise en œuvre. L'analyse prédictive des résultats des lots montre généralement un retour sur investissement dans les 6 à 12 mois grâce à la réduction des échecs des lots et à l'amélioration du rendement. Les initiatives d'optimisation des processus peuvent nécessiter 12 à 24 mois mais génèrent une valeur continue. Les avantages financiers proviennent de l'amélioration du rendement, de l'accélération du développement, de la réduction des temps d'arrêt et de l'accélération de la libération des lots.
Conclusion
La transformation numérique modifie fondamentalement le fonctionnement des bioprocédés. Les technologies ne sont plus spéculatives - l'intelligence artificielle, les jumeaux numériques et l'analyse en temps réel donnent des résultats mesurables chez les principaux fabricants.
Mais le succès ne se limite pas à l'adoption d'une technologie. Les organisations ont besoin d'une infrastructure de données, d'une collaboration interfonctionnelle, de cadres de conformité réglementaire et de stratégies de mise en œuvre claires. En commençant par des projets pilotes ciblés dans des domaines à forte valeur ajoutée, elles renforcent leurs capacités tout en démontrant le retour sur investissement.
Le paysage concurrentiel exige une amélioration continue. Les fabricants qui exploitent efficacement les outils numériques acquièrent des avantages en termes de rapidité, d'efficacité et de qualité que leurs concurrents ont du mal à égaler.
Prêt à transformer vos opérations de biotraitement ? Commencez par évaluer votre infrastructure de données actuelle et identifiez les cas d'utilisation à fort impact pour lesquels les solutions numériques peuvent apporter des gains rapides. Construisez à partir de là avec une feuille de route claire qui équilibre l'ambition avec des considérations pratiques de mise en œuvre.


