Résumé rapide : La transformation numérique dans le domaine de la thérapie cellulaire et génique s'appuie sur des technologies de fabrication avancées, des plateformes d'IA/ML, des jumeaux numériques et des systèmes de données intégrés pour accélérer les délais de développement, améliorer la qualité des produits, améliorer les résultats pour les patients et faire évoluer la production des thérapies autologues vers les thérapies allogéniques. Selon les directives de la FDA, ces innovations permettent de relever les défis critiques de la fabrication tout en maintenant la conformité réglementaire et la fiabilité de la chaîne d'approvisionnement.
Les thérapies cellulaires et géniques sont passées du stade de traitements expérimentaux à celui de réalités commerciales. Mais la mise à l'échelle de ces médicaments personnalisés présente des défis sans précédent en matière de fabrication, de réglementation et de logistique.
La transformation numérique offre des solutions. De l'appariement des patients piloté par l'IA aux jumeaux numériques prédisant la réponse au traitement, la technologie remodèle chaque étape de la chaîne de valeur de la CGT.
Voici comment l'innovation numérique fait progresser le développement, la fabrication et la distribution des thérapies cellulaires et géniques, et ce que cela signifie pour les patients et les prestataires de soins.
Le paysage du marché de la CGT et les impératifs numériques
Selon des estimations mondiales, le marché de la thérapie cellulaire et génique atteindra $93,78 milliards d'euros d'ici 2030. Cette croissance explosive crée des besoins opérationnels urgents.
Les flux de travail traditionnels basés sur le papier ne peuvent pas suivre le rythme. Les processus manuels introduisent des erreurs, ralentissent les cycles de production et compromettent l'intégrité des données - des problèmes critiques lorsqu'il s'agit de fabriquer des thérapies spécifiques aux patients dans des délais serrés.
La FDA a reconnu ces défis. Grâce à son programme de désignation des technologies de fabrication avancées, l'agence encourage l'adoption rapide de technologies qui améliorent la fiabilité de la fabrication et optimisent les délais de développement des médicaments et des produits biologiques.
La transformation numérique permet de relever les principaux défis de la CGT :
- Coordination complexe de la chaîne d'approvisionnement entre les sites de collecte, les installations de fabrication et les centres de traitement
- Maintien de la chaîne d'identité et de la chaîne de conservation pour les produits autologues
- Contrôle de la qualité en temps réel et tests de validation
- Documentation sur la conformité réglementaire et pistes d'audit
- Programmation des patients et gestion de la chronologie de la veine à la veine
Les enjeux sont considérables. Les taux d'échec des traitements restent importants, même avec des thérapies prometteuses - la thérapie CD19-CAR permet d'obtenir des taux de rémission de 70-90% dans les cancers hématologiques, mais de nombreux patients finissent par rechuter en raison de la régulation négative de l'antigène et des mécanismes d'évasion de la tumeur.
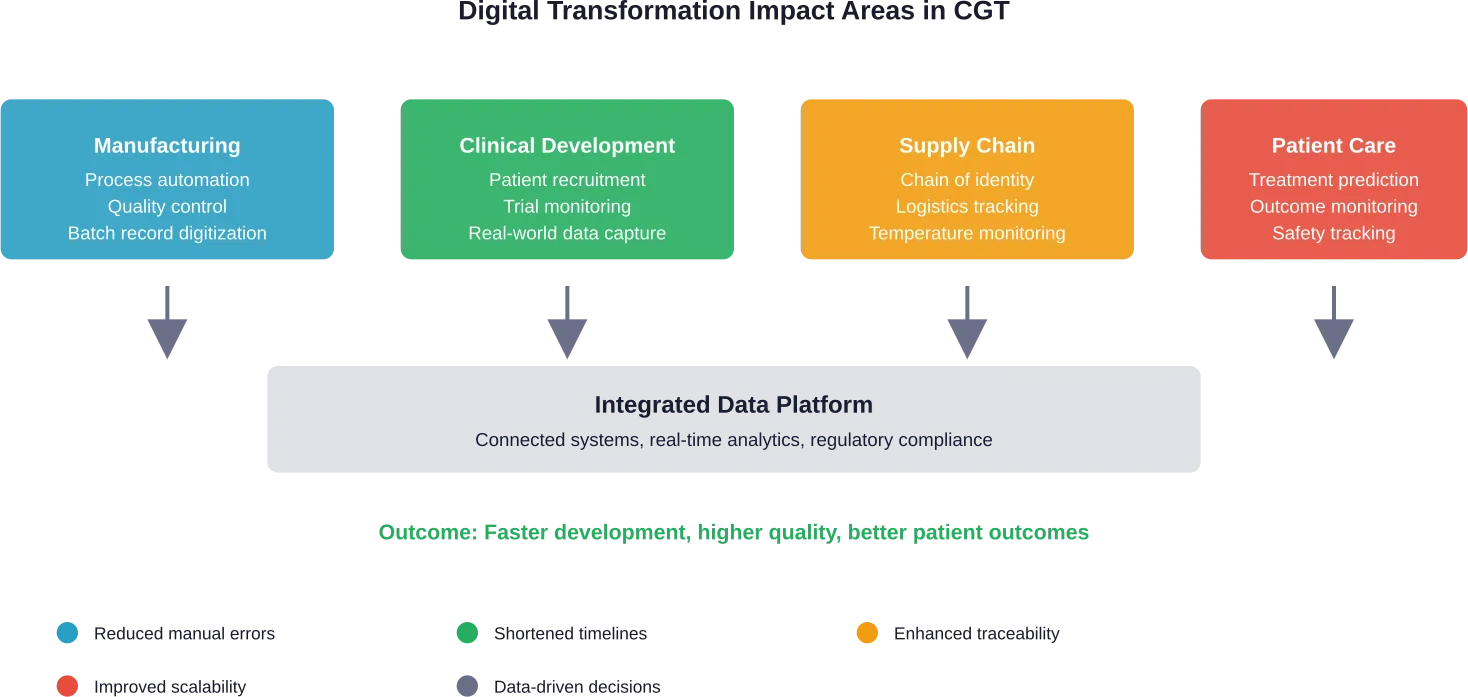
Les technologies de fabrication avancées remodèlent la production
La FDA définit la fabrication avancée comme “un terme collectif désignant les nouvelles technologies de fabrication de produits médicaux susceptibles d'améliorer la qualité des médicaments, de remédier aux pénuries de médicaments et d'accélérer la mise sur le marché”.”
Pour la CGT en particulier, la fabrication avancée englobe le traitement en continu, les plates-formes d'automatisation, la technologie d'analyse des processus et les systèmes de contrôle de la qualité en temps réel.
Dossiers de lots électroniques et automatisation des processus
Le remplacement des dossiers de lot sur papier représente une étape fondamentale de la transformation numérique. Les dossiers de lot électroniques éliminent les erreurs de transcription, offrent une visibilité en temps réel des processus et créent automatiquement une documentation prête à être auditée.
Les principales organisations font état d'avantages significatifs :
- Réduction des temps de cycle de fabrication grâce à l'automatisation des transitions du flux de travail
- Amélioration de l'intégrité des données grâce aux signatures électroniques et à la vérification de l'horodatage
- Libération plus rapide des lots grâce à des processus intégrés d'examen de la qualité
- Amélioration de la collaboration entre les sites de production et les sponsors
Mais une mise en œuvre réussie ne se limite pas au déploiement d'un logiciel. Les organisations doivent repenser les flux de travail, former le personnel et intégrer les systèmes dans les fonctions de qualité, de fabrication et de réglementation.
Systèmes de chaîne d'identité et de chaîne de possession
Les thérapies autologues exigent une certitude absolue que le bon produit atteint le bon patient. Les systèmes de chaînes d'identité numériques utilisent la vérification biométrique, le suivi RFID et la lecture de codes-barres pour assurer la traçabilité des produits, de la collecte à la perfusion.
Ces systèmes s'intègrent aux plateformes de planification, aux fournisseurs de services logistiques et aux systèmes d'information des hôpitaux, créant ainsi une visibilité de bout en bout tout en réduisant les étapes de vérification manuelle qui ralentissent les délais de production.
Technologie analytique des procédés et libération en temps réel
Les tests de qualité traditionnels sont effectués à la fin de lots distincts. La technologie analytique des procédés permet de contrôler en continu les attributs de qualité critiques au cours de la production.
La collecte de données en temps réel permet de prendre des décisions plus rapides et d'identifier les écarts avant qu'ils ne compromettent la qualité du produit. Certaines installations de pointe mettent en œuvre des tests de libération en temps réel, où les données de surveillance continue remplacent les tests sur les produits finis, ce qui permet de raccourcir considérablement les délais de libération.
Les jumeaux numériques et l'optimisation des traitements par l'IA
La technologie des jumeaux numériques crée des répliques virtuelles de systèmes biologiques, permettant ainsi la simulation et la prédiction avant l'intervention physique. Pour la thérapie cellulaire et génique, les jumeaux numériques fonctionnent à plusieurs échelles.
Jumeaux numériques au niveau du patient
Des recherches publiées dans des revues médicales démontrent que les jumeaux numériques peuvent prédire les résultats de la thérapie cellulaire CAR-T en intégrant des données génomiques, des résultats d'imagerie, des informations provenant de capteurs portables et des dossiers cliniques dans des simulations à plusieurs échelles.
Ces modèles spécifiques aux patients aident les cliniciens :
- Prédire la réponse au traitement en fonction des caractéristiques individuelles de la tumeur et des profils immunitaires
- Optimiser les stratégies de dosage pour équilibrer l'efficacité et les risques de toxicité
- Identifier les patients les plus susceptibles de bénéficier d'approches thérapeutiques spécifiques
- Contrôler la réponse après le traitement et détecter les signes précoces de rechute
Les algorithmes d'apprentissage automatique formés sur les données historiques des patients améliorent la précision des prédictions au fil du temps. Au fur et à mesure que les ensembles de données augmentent, les jumeaux numériques deviennent de plus en plus précis dans la prévision des trajectoires de traitement individuelles.
Processus de fabrication Jumeaux numériques
Au-delà des soins aux patients, les jumeaux numériques modélisent les processus de fabrication. Les simulations de production virtuelle permettent d'identifier les paramètres de processus optimaux, de prédire les résultats en termes de rendement et de tester les changements de processus sans consommer le matériel réel du patient.
Cette capacité s'avère particulièrement précieuse lors du transfert de technologie, lorsqu'il s'agit de déplacer des processus entre des installations de développement et de fabrication commerciale ou de passer d'un petit volume de production à un grand volume.
Innovation en matière d'essais cliniques grâce aux technologies numériques
Les technologies numériques transforment la manière dont les essais cliniques sont conçus, menés et contrôlés, ce qui est particulièrement important étant donné les populations limitées de patients pour de nombreuses indications de la CGT.
Composantes de l'essai décentralisé
Alors que l'administration de la CGT nécessite des installations spécialisées, les outils numériques permettent la surveillance à distance des patients, les consultations virtuelles et le prélèvement d'échantillons à domicile, le cas échéant.
Des dispositifs portables permettent de suivre les paramètres de sécurité en continu plutôt qu'à l'occasion de visites cliniques distinctes. Les résultats rapportés par les patients sont directement intégrés dans les bases de données des essais par le biais d'applications mobiles. Les plateformes de télémédecine permettent des contrôles fréquents sans frais de déplacement.
Intégration de données dans le monde réel
L'American Society of Gene & Cell Therapy a récemment soumis des commentaires en faveur des normes Health Level Seven Fast Healthcare Interoperability Resources (HL7 FHIR) pour l'intégration des données dans le monde réel.
Les données réelles issues des dossiers médicaux électroniques, des demandes d'indemnisation et des registres de patients complètent les informations traditionnelles des essais cliniques, en fournissant des informations sur la sécurité à long terme, l'efficacité dans des populations plus larges et les résultats comparatifs des traitements.
La FDA étudie des cadres permettant d'intégrer des données du monde réel dans la prise de décision réglementaire, en particulier pour le suivi de la sécurité après l'approbation et les considérations relatives à l'extension de l'étiquetage.
Plans d'essais adaptatifs
Les plateformes de données numériques permettent de concevoir des essais adaptatifs qui modifient les protocoles en fonction de l'accumulation de données. Pour les indications de maladies rares avec des populations de patients limitées, les approches adaptatives maximisent le gain d'informations tout en minimisant l'exposition des patients à des traitements inefficaces.
Les essais de phase précoce combinent de plus en plus les objectifs des phases 1 et 2, en se concentrant simultanément sur la sécurité et l'efficacité préliminaire. Cette approche rationalisée est scientifiquement justifiée et éthiquement appropriée compte tenu des besoins urgents non satisfaits.
Considérations réglementaires et cadres de conformité
La transformation numérique doit s'aligner sur l'évolution des attentes réglementaires. La FDA a publié des orientations sur les technologies de fabrication avancées, l'intelligence artificielle dans les dispositifs médicaux et les technologies de santé numérique dans les essais cliniques.
Titre sur les technologies de fabrication avancées
La FDA a publié les orientations finales pour le programme de désignation des technologies de fabrication avancées en décembre 2024. Ce cadre permet aux fabricants de demander la désignation de technologies spécifiques qui ont le potentiel d'améliorer la qualité des produits, de réduire les risques de fabrication ou de remédier aux pénuries de médicaments.
Les technologies désignées font l'objet d'un engagement renforcé de la part de la FDA, avec notamment des réunions pour discuter des plans de développement, des évaluations de la fabrication et des voies réglementaires. Cette collaboration proactive aide les organisations à mettre en œuvre de nouvelles technologies tout en respectant la réglementation.
Intégrité des données et validation du système
Les systèmes numériques doivent répondre à des exigences rigoureuses en matière d'intégrité des données. Les enregistrements électroniques doivent être accompagnés de pistes d'audit documentant toutes les créations, modifications et suppressions de données. L'accès au système nécessite des contrôles basés sur les rôles et un examen régulier.
La validation des systèmes informatiques démontre que les plateformes numériques fonctionnent toujours comme prévu. Les protocoles de validation documentent les exigences du système, les procédures de test et le contrôle continu, créant ainsi la preuve que les systèmes maintiennent l'intégrité des données tout au long de leur cycle de vie.
Supervision de l'IA et de l'apprentissage automatique
À mesure que les technologies de l'IA s'intègrent dans le développement et la fabrication de produits de haute technologie, les cadres réglementaires s'adaptent. La FDA reconnaît que les systèmes d'IA/ML impliquent des “processus complexes et dynamiques” nécessitant des approches de surveillance différentes de celles des logiciels traditionnels.
Les éléments clés à prendre en compte sont la transparence des algorithmes, la représentativité des données d'entraînement, le contrôle des performances lors du déploiement et les procédures de contrôle des modifications lorsque les modèles sont mis à jour sur la base de nouvelles données.
Surmonter les obstacles à la mise en œuvre
Malgré des avantages évidents, la transformation numérique se heurte à des obstacles. Comprendre les obstacles les plus courants permet aux organisations d'élaborer des stratégies d'atténuation.
Résistance culturelle et organisationnelle
Le passage de flux de travail sur papier à des systèmes numériques nécessite un changement culturel. Le personnel habitué aux processus traditionnels peut résister aux nouvelles approches, en particulier si la formation est inadéquate ou si les avantages ne sont pas clairement communiqués.
Les mises en œuvre réussies donnent la priorité à la gestion du changement :
- Impliquer les utilisateurs finaux dans la sélection des technologies et la conception des flux de travail
- Fournir une formation complète avec des possibilités de mise en pratique
- Identifier et responsabiliser les champions du numérique dans chaque domaine fonctionnel
- Célébrer les premiers succès et partager largement les expériences réussies
- Répondre aux préoccupations de manière transparente et ajuster la mise en œuvre en fonction du retour d'information.
Complexité de l'intégration des systèmes
Les organisations de la CGT exploitent de multiples systèmes spécialisés - systèmes d'exécution de la fabrication, systèmes de gestion des informations de laboratoire, plateformes de planification des ressources de l'entreprise, systèmes de gestion des essais cliniques, et bien d'autres encore.
La création d'un flux de données transparent entre ces systèmes nécessite une architecture d'intégration soignée. Les interfaces de programmation d'applications permettent la communication de système à système, mais les projets d'intégration exigent des ressources techniques et des tests importants.
De nombreuses organisations adoptent des approches progressives, en donnant la priorité aux intégrations à forte valeur ajoutée plutôt que d'essayer d'établir une connexion complète immédiatement.
Contraintes de ressources et incertitude du retour sur investissement
La transformation numérique nécessite un investissement initial dans les logiciels, l'infrastructure, les services de conseil et le temps du personnel. Pour les petites organisations ou celles qui développent des thérapies pour des maladies très rares, les contraintes de ressources peuvent retarder ou empêcher l'adoption.
L'élaboration d'analyses de rentabilité claires permet d'obtenir des financements. La quantification des avantages escomptés - réduction des temps de cycle, diminution des taux d'erreur, amélioration des rendements, accélération des soumissions réglementaires - crée des projections tangibles de retour sur investissement qui justifient l'investissement.
Les modèles de logiciels en nuage (Software-as-a-Service) réduisent les besoins en capitaux initiaux par rapport aux systèmes sur site, ce qui rend les outils numériques plus accessibles aux organisations dont les budgets sont limités.
| Zone de défi | Obstacles courants | Stratégies d'atténuation |
|---|---|---|
| Choix de la technologie | Un paysage de fournisseurs pléthorique, une différenciation des fonctionnalités peu claire | Définir d'abord les besoins, procéder à des essais pilotes avant de s'engager pleinement, rechercher des références auprès de pairs. |
| Migration des données | Problèmes de qualité des données héritées, incompatibilités de format | Nettoyer les données de manière proactive, établir des protocoles de validation de la migration, accepter une approche par étapes |
| Conformité réglementaire | Incertitude quant aux exigences de validation, préoccupations quant à l'état de préparation à l'audit | S'engager très tôt dans une démarche de qualité/réglementation, s'appuyer sur les kits de validation des fournisseurs, documenter de manière exhaustive. |
| Formation du personnel | Contraintes de temps, niveaux de compétence technique variables | Parcours de formation basés sur les rôles, modèle de super-utilisateur, ressources d'assistance permanente |
| Gestion des fournisseurs | Relations avec de multiples fournisseurs, dépendances d'intégration | Donner la priorité aux plates-formes dotées d'API ouvertes, établir une gouvernance claire, tenir à jour les tableaux de bord des fournisseurs. |
Accessibilité globale et considérations relatives à l'équité en matière de santé
La transformation numérique doit prendre en compte les problèmes d'accessibilité au niveau mondial. L'application des thérapies cellulaires et géniques dans les pays à faibles et moyens revenus se heurte à des obstacles importants.
Entre 1991 et 2008, seuls 2% environ des 274 000 essais cliniques mondiaux ont été menés en Afrique, malgré la charge de morbidité considérable que représente ce continent. La capacité réglementaire limitée, les lacunes en matière d'infrastructures et les contraintes en matière de ressources entravent l'accès aux thérapies avancées.
Les technologies numériques offrent des solutions partielles :
- Les plateformes de télémédecine permettent de consulter des spécialistes à distance sans déplacement coûteux
- Les systèmes réglementaires basés sur l'informatique dématérialisée réduisent les besoins en infrastructures locales
- Des réseaux de fabrication partagés pourraient desservir efficacement plusieurs régions
- Les programmes de formation numérique renforcent les capacités locales sans nécessiter le déplacement d'experts.
Toutefois, la technologie seule ne permet pas de remédier aux inégalités fondamentales en matière d'accès aux soins de santé, de mécanismes de financement et de capacité industrielle. La transformation numérique doit compléter - et non remplacer - les efforts plus larges visant à démocratiser l'accès aux thérapies innovantes à l'échelle mondiale.
Orientations futures et technologies émergentes
L'innovation numérique dans la CGT continue de s'accélérer. Plusieurs technologies émergentes sont particulièrement prometteuses.
Blockchain pour la vérification de la chaîne d'approvisionnement
La technologie de registre distribué Blockchain crée des enregistrements immuables de la manipulation des produits, des conditions de stockage et des transferts de garde. Pour les thérapies autologues nécessitant une garantie absolue de la chaîne d'identité, la blockchain offre une traçabilité vérifiée par cryptographie.
Les premières mises en œuvre démontrent la faisabilité, bien que l'adoption généralisée attende la normalisation et l'intégration avec les systèmes existants.
Analyse avancée et fabrication prédictive
Les modèles d'apprentissage automatique formés sur les données historiques de fabrication peuvent prédire les résultats des lots, identifier les écarts de processus avant qu'ils n'aient un impact sur la qualité et recommander des ajustements de paramètres pour optimiser le rendement.
Au fur et à mesure que les ensembles de données de fabrication augmentent, les capacités prédictives s'améliorent, ce qui pourrait permettre une fabrication sans interruption avec une intervention humaine minimale pour les étapes de production de routine.
Biologie synthétique et conception computationnelle
Les outils informatiques accélèrent la conception des thérapies cellulaires. Plutôt que de procéder à des essais empiriques, les approches de biologie synthétique utilisent la modélisation pour concevoir des circuits génétiques, prédire le comportement des cellules et optimiser les constructions thérapeutiques in silico avant de les tester physiquement.
Cette capacité de conception informatique complète les jumeaux numériques, créant ainsi des environnements virtuels complets pour le développement et l'optimisation des thérapies.
Feuille de route pratique pour la mise en œuvre
Les organisations qui entament une transformation numérique devraient suivre des approches structurées plutôt que d'adopter des technologies au coup par coup.
Étape 1 : Évaluer la situation actuelle
Documenter les processus, systèmes et flux de données existants. Identifier les points douloureux, les inefficacités et les risques de non-conformité. Évaluer la maturité numérique dans les fonctions de fabrication, de qualité, cliniques et commerciales.
Étape 2 : Définir la vision stratégique
Établir des objectifs clairs alignés sur les priorités de l'entreprise. Quels résultats spécifiques la transformation numérique doit-elle atteindre ? Un délai de mise sur le marché plus rapide ? Amélioration de la qualité des produits ? De meilleurs résultats pour les patients ? Réduction des coûts de production ?
Hiérarchiser les cas d'utilisation en fonction de l'impact attendu et de la faisabilité de la mise en œuvre.
Étape 3 : Sélectionner les technologies appropriées
Évaluer les plateformes en fonction des exigences définies. Tenez compte des capacités d'intégration, de la stabilité du fournisseur, des caractéristiques de conformité réglementaire, de l'évolutivité et du coût total de possession.
Éviter les approches qui privilégient la technologie et sélectionnent les outils avant de comprendre les besoins.
Étape 4 : Exécuter des projets pilotes ciblés
Tester les technologies sélectionnées dans un cadre contrôlé avant de les déployer à l'échelle de l'entreprise. Les projets pilotes permettent de valider les avantages escomptés, d'identifier les difficultés de mise en œuvre et de renforcer la confiance de l'organisation.
Documenter les enseignements tirés et affiner les approches avant de passer à l'échelle supérieure.
Étape 5 : Transposer les initiatives réussies à une plus grande échelle
Étendre les projets pilotes qui ont fait leurs preuves à d'autres sites, produits ou fonctions. Investir dans la formation, la gestion du changement et l'infrastructure de soutien permanent.
Établir des cadres de gouvernance garantissant un déploiement cohérent et empêchant les modifications non autorisées du système.
Étape 6 : Optimiser en permanence
Surveillez les mesures de performance, recueillez les commentaires des utilisateurs et affinez les processus de manière itérative. La transformation numérique n'est pas un projet ponctuel, c'est une capacité permanente qui nécessite une attention continue.
Se tenir au courant des technologies émergentes et de l'évolution des attentes en matière de réglementation par le biais d'associations sectorielles, de conférences et de réseaux de pairs.
| Phase de mise en œuvre | Durée typique | Principaux résultats attendus | Mesures de réussite |
|---|---|---|---|
| L'évaluation | 1-2 mois | Documentation de l'état actuel, analyse des lacunes, évaluation de la maturité | Compréhension globale des capacités de base |
| Développement de la stratégie | 1-2 mois | Déclaration de vision, cas d'utilisation classés par ordre de priorité, feuille de route, analyse de rentabilité | Alignement de l'exécutif et approbation du financement |
| Choix de la technologie | 2-3 mois | Document d'exigences, évaluation des fournisseurs, décision de sélection | Choix de la plate-forme en fonction des besoins |
| Exécution du projet pilote | 3-6 mois | Système configuré, utilisateurs formés, résultats du projet pilote, enseignements tirés | Avantages validés, approche de mise en œuvre affinée |
| Déploiement à l'échelle | 6-18 mois | Déploiement de l'entreprise, formation élargie, achèvement de l'intégration | Objectifs d'adoption, amélioration des performances |
| Optimisation continue | En cours | Tableaux de bord des performances, révisions régulières, carnet de commandes des améliorations | Avantages durables, satisfaction des utilisateurs, évolution des capacités |
Créer des bases numériques fiables pour la thérapie cellulaire et génique
Les travaux de thérapie cellulaire et génique dépendent de données précises, de processus traçables et de systèmes capables de gérer à la fois la recherche et la production sans rupture de continuité. A-listware aide les organisations en examinant la façon dont les données, les systèmes et les flux de travail sont actuellement structurés, puis en les réorganisant pour améliorer la cohérence et le contrôle.
Il s'agit souvent de renforcer la façon dont les informations sont stockées et accessibles, de réduire les transferts manuels et de veiller à ce que les systèmes puissent soutenir la croissance sans créer de lacunes entre les différentes étapes du travail. Si votre configuration actuelle vous empêche de garder le contrôle ou d'évoluer en toute sécurité, contactez Logiciel de liste A pour obtenir une vision claire et pratique de la manière d'aller de l'avant.
Mesurer le succès de la transformation numérique
Des mesures quantifiables démontrent la valeur de la transformation et guident l'amélioration continue.
Les mesures de fabrication comprennent la réduction du temps de cycle, les taux de réussite des lots, la fréquence des déviations et le délai de mise à disposition. Les organisations les plus performantes font état d'améliorations dans ces domaines à la suite de la numérisation.
Les mesures de qualité permettent de suivre les taux d'erreur, les délais d'enquête, les résultats d'audit et les résultats d'inspection. Les systèmes électroniques réduisent généralement les erreurs de documentation de 60 à 80% par rapport aux processus papier.
Les indicateurs cliniques mesurent les taux de recrutement des patients, la fréquence des déviations de protocole, les scores de qualité des données et l'efficacité du suivi. Les outils numériques peuvent réduire les délais de recrutement de 30% ou plus.
Les indicateurs financiers comprennent le coût par lot, les coûts de possession des stocks, la productivité de la main-d'œuvre et le retour sur investissement numérique. Les transformations complètes permettent généralement d'obtenir un retour sur investissement positif dans un délai de 18 à 36 mois.
Questions fréquemment posées
- Quels sont les plus grands défis à relever pour transformer numériquement la fabrication des thérapies cellulaires et géniques ?
Les principaux défis sont la complexité de l'intégration des systèmes sur de multiples plateformes spécialisées, la résistance culturelle du personnel habitué aux flux de travail sur papier, les contraintes de ressources limitant l'investissement initial, l'incertitude quant à la conformité réglementaire des nouvelles technologies et la migration des données à partir des systèmes existants. Les organisations surmontent ces obstacles grâce à des mises en œuvre progressives, à une gestion rigoureuse du changement, à une démonstration claire du retour sur investissement et à un engagement réglementaire précoce.
- Comment les jumeaux numériques améliorent-ils les résultats de la thérapie cellulaire CAR-T ?
Les jumeaux numériques créent des modèles virtuels spécifiques au patient en intégrant les données génomiques, les caractéristiques de la tumeur, les profils immunitaires, les résultats d'imagerie et les antécédents cliniques. Ces simulations à plusieurs échelles permettent de prédire la réponse individuelle au traitement, d'optimiser les stratégies de dosage, d'identifier les patients les plus susceptibles d'en bénéficier et de détecter rapidement les signaux de rechute. Les algorithmes d'apprentissage automatique améliorent la précision des prédictions au fur et à mesure que les ensembles de données augmentent, ce qui rend les jumeaux numériques de plus en plus précieux pour la personnalisation des approches thérapeutiques.
- Quelles sont les orientations réglementaires pour les technologies de fabrication avancées dans la CGT ?
La FDA a finalisé en décembre 2024 des lignes directrices établissant le programme de désignation des technologies de fabrication avancées (Advanced Manufacturing Technologies Designation Program). Ce cadre permet aux fabricants de demander la désignation de technologies qui améliorent la qualité, réduisent les risques ou remédient aux pénuries. Les technologies désignées bénéficient d'un engagement renforcé de la FDA, y compris des réunions de développement et des discussions sur la voie réglementaire. D'autres orientations portent sur l'IA/ML dans les dispositifs médicaux, les technologies de santé numérique dans les essais et les exigences en matière d'intégrité des données pour les systèmes électroniques.
- Combien de temps la transformation numérique prend-elle généralement pour les organisations de thérapie cellulaire et génique ?
Les délais varient en fonction de la portée et de l'état de préparation de l'organisation. L'évaluation initiale et l'élaboration de la stratégie prennent de 2 à 4 mois. La sélection de la technologie ajoute 2 à 3 mois. Les projets pilotes durent de 3 à 6 mois. Le déploiement à l'échelle de l'entreprise s'étend sur 6 à 18 mois pour une transformation complète. Toutefois, les organisations doivent considérer qu'il s'agit d'une évolution continue plutôt que de projets finis - l'optimisation continue se poursuit indéfiniment à mesure que les technologies et les besoins évoluent.
- Les petites entreprises de biotechnologie peuvent-elles se permettre des initiatives de transformation numérique ?
Oui, bien que les approches diffèrent de celles des grandes entreprises pharmaceutiques. Les plateformes de logiciels en tant que service basées sur l'informatique en nuage réduisent les besoins en capitaux par rapport aux systèmes sur site. Les mises en œuvre ciblées sur les cas d'utilisation à forte valeur ajoutée offrent des avantages sans déploiement global à l'échelle de l'entreprise. Les organisations de développement et de fabrication sous contrat offrent de plus en plus de services numériques, ce qui permet aux petites entreprises d'accéder à des capacités avancées sans avoir à mettre en place une infrastructure interne. Les approches progressives permettent d'étaler les coûts dans le temps tout en apportant une valeur incrémentale.
- Comment la numérisation améliore-t-elle la gestion de la chaîne d'approvisionnement pour les thérapies autologues ?
Les plateformes numériques de la chaîne d'approvisionnement intègrent dans des systèmes unifiés la programmation des sites de collecte, le suivi logistique, les mises à jour de l'état de la fabrication et la coordination des centres de traitement. La visibilité en temps réel permet une gestion proactive des exceptions plutôt qu'une lutte réactive contre les incendies. Les systèmes de chaîne d'identité utilisant la vérification biométrique, les étiquettes RFID et la lecture des codes-barres garantissent la traçabilité des produits, de l'aphérèse à la perfusion. La surveillance de la température, l'optimisation des itinéraires et la documentation automatisée réduisent les erreurs tout en accélérant les délais entre la veine et la veine de 15-30%.
- Quel rôle jouent les données réelles dans le développement des thérapies cellulaires et géniques ?
Les données du monde réel provenant des dossiers médicaux électroniques, des bases de données sur les réclamations et des registres de patients permettent de mieux comprendre l'innocuité à long terme, l'efficacité dans diverses populations et les résultats comparatifs des traitements au-delà des essais contrôlés. La FDA élabore des cadres pour intégrer les données du monde réel dans les décisions réglementaires, en particulier pour le suivi de la sécurité après l'approbation, les extensions d'étiquetage et les indications de maladies rares pour lesquelles les essais traditionnels posent des problèmes de recrutement. Les formats de données normalisés tels que HL7 FHIR permettent une intégration efficace des données du monde réel dans les programmes de développement.
Conclusion
La transformation numérique représente plus que l'adoption d'une technologie - il s'agit d'une réimagination fondamentale de la façon dont les thérapies cellulaires et géniques sont développées, fabriquées et délivrées aux patients.
De la prédiction des traitements par l'IA aux plateformes de fabrication automatisées, les outils numériques relèvent les défis critiques qui limitent l'évolutivité et l'accessibilité de la CGT. Les organisations qui mettent en œuvre ces technologies font état de délais de développement plus courts, d'une meilleure qualité des produits, d'une réduction des coûts et de meilleurs résultats pour les patients.
Pourtant, la technologie seule ne garantit pas le succès. Une transformation efficace nécessite une vision stratégique, une collaboration interfonctionnelle, un alignement réglementaire, une gestion du changement et une optimisation continue. Les organisations doivent trouver un équilibre entre l'innovation et la conformité, la rapidité et la qualité, et l'automatisation et la supervision humaine.
Le soutien de la FDA aux technologies de fabrication avancées par le biais de programmes de désignation et d'un engagement renforcé crée des environnements réglementaires favorables à l'innovation. À mesure que les capacités numériques mûrissent et que leur adoption s'étend, la thérapie cellulaire et génique tiendra de plus en plus sa promesse de traitements curatifs pour des affections jusqu'alors incurables.
Le moment est venu pour les organisations de la CGT d'évaluer leur maturité numérique, d'identifier les opportunités à forte valeur ajoutée et d'entamer leur parcours de transformation. Les avantages concurrentiels et les bénéfices pour les patients font que la transformation numérique n'est pas seulement bénéfique, mais essentielle.
Prêt à faire progresser la transformation numérique de votre organisation ? Commencez par évaluer vos capacités actuelles par rapport aux références du secteur, en identifiant les points douloureux ayant un impact commercial mesurable, et en donnant la priorité aux initiatives permettant d'obtenir des gains rapides tout en construisant un changement global.


