Короткий виклад: Цифрова трансформація в клітинній та генній терапії використовує передові виробничі технології, платформи AI/ML, цифрових двійників та інтегровані системи даних для прискорення термінів розробки, підвищення якості продукції, покращення результатів лікування пацієнтів та масштабування виробництва від аутологічної до алогенної терапії. Згідно з рекомендаціями FDA, ці інновації вирішують критичні виробничі проблеми, зберігаючи при цьому відповідність регуляторним нормам і надійність ланцюжка поставок.
Клітинна та генна терапія перейшла від експериментальних методів лікування до комерційних реалій. Але масштабування цих персоналізованих ліків пов'язане з безпрецедентними виробничими, регуляторними та логістичними проблемами.
Цифрова трансформація пропонує рішення. Від підбору пацієнтів на основі штучного інтелекту до цифрових двійників, які прогнозують реакцію на лікування, технології змінюють кожен етап ланцюжка створення вартості ТГТ.
Ось як цифрові інновації сприяють розвитку клітинної та генної терапії, виробництву та доставці - і що це означає для пацієнтів та лікарів.
Ландшафт ринку УГТ та цифрові імперативи
За глобальними оцінками, до 2030 року ринок клітинної та генної терапії досягне 1 трлн. 93,78 млрд. доларів США. Таке стрімке зростання створює нагальні операційні потреби.
Традиційні паперові робочі процеси не встигають за часом. Ручні процеси призводять до помилок, сповільнюють виробничі цикли та порушують цілісність даних, що є критично важливими при розробці індивідуальної терапії для конкретного пацієнта в стислі терміни.
FDA визнає ці виклики. Через свою Програму призначення передових виробничих технологій агентство заохочує раннє впровадження технологій, які підвищують надійність виробництва та оптимізують терміни розробки лікарських та біологічних препаратів.
Цифрова трансформація вирішує основні проблеми CGT:
- Комплексна координація ланцюга постачання між пунктами збору, виробничими потужностями та центрами переробки
- Підтримання ланцюга ідентифікації та ланцюга відповідального зберігання для аутологічних продуктів
- Моніторинг якості та тестування релізів у реальному часі
- Документація щодо дотримання нормативних вимог та аудиторські сліди
- Планування пацієнтів та управління графіком "від вени до вени
Ставки високі. Показники невдач лікування залишаються значними навіть при застосуванні перспективних методів лікування - терапія CD19-CAR досягає рівня ремісії 70-90% при гематологічних раках, проте у багатьох пацієнтів з часом виникає рецидив через зниження регуляції антигенів та механізми ухилення від пухлинного процесу.
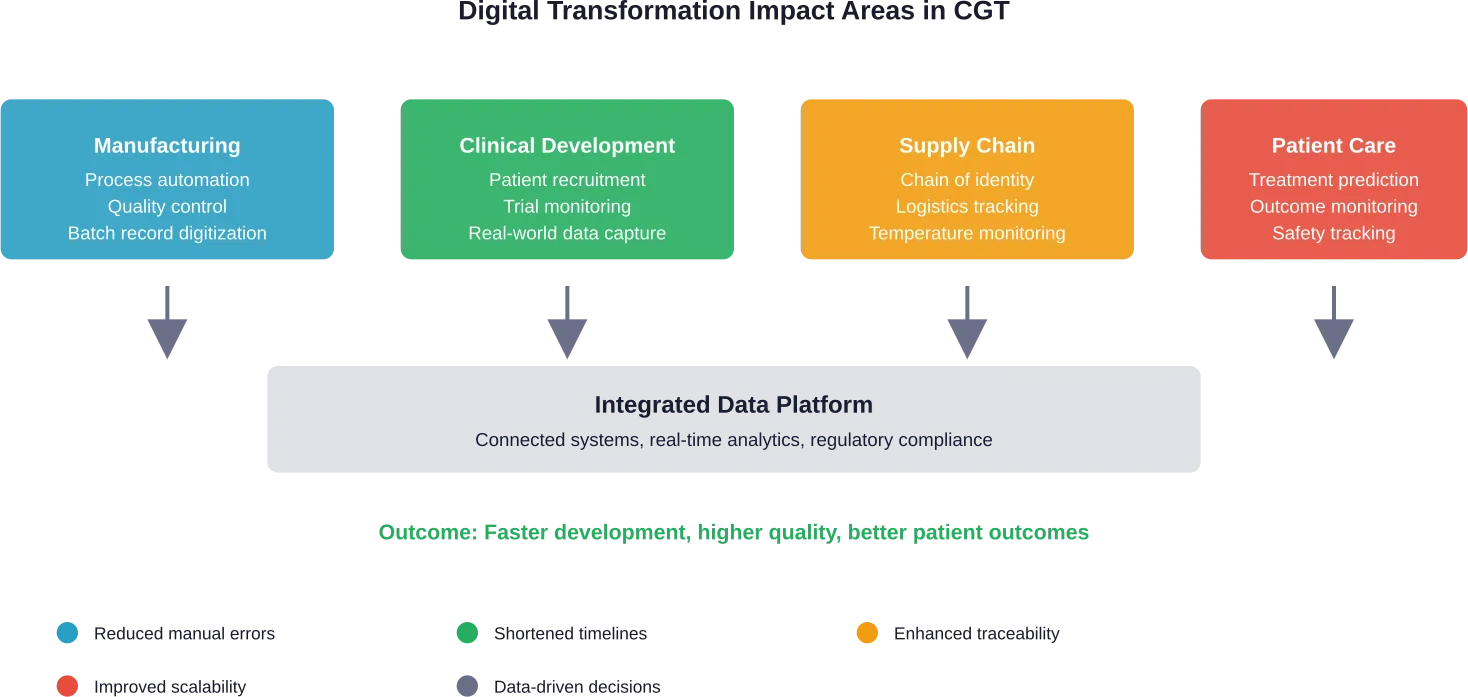
Передові виробничі технології переформатовують виробництво
FDA визначає передове виробництво як “збірний термін для позначення нових технологій виробництва медичних препаратів, які можуть покращити якість ліків, вирішити проблему дефіциту ліків та пришвидшити час виходу на ринок”.”
Зокрема, для ПГУ передове виробництво охоплює безперервну обробку, платформи автоматизації, технологію аналізу процесів і системи моніторингу якості в реальному часі.
Електронний облік партій та автоматизація процесів
Заміна паперового документообігу є фундаментальним кроком цифрової трансформації. Електронні записи усувають помилки транскрипції, забезпечують видимість процесу в реальному часі та автоматично створюють документацію, готову до аудиту.
Провідні організації повідомляють про значні переваги:
- Скорочення часу виробничого циклу завдяки автоматизованим переходам робочого процесу
- Покращена цілісність даних завдяки електронним підписам та перевірці часових міток
- Швидший випуск партій завдяки інтегрованим процесам перевірки якості
- Посилення співпраці між виробничими майданчиками та спонсорами
Але успішне впровадження вимагає більше, ніж просто розгортання програмного забезпечення. Організації повинні перепроектувати робочі процеси, навчити персонал та інтегрувати системи у функції контролю якості, виробництва та регулювання.
Системи ідентифікації та управління ланцюгами поставок
Аутологічна терапія вимагає абсолютної впевненості в тому, що потрібний продукт потрапляє до потрібного пацієнта. Цифрові ланцюжки систем ідентифікації використовують біометричну верифікацію, відстеження за допомогою радіочастотної ідентифікації (RFID) і сканування штрих-кодів, щоб забезпечити відстеження продукту від моменту збору до інфузії.
Ці системи інтегруються з платформами планування, постачальниками логістичних послуг та лікарняними інформаційними системами, створюючи наскрізну прозорість і зменшуючи кількість ручних перевірок, які сповільнюють виробничі терміни.
Технологія аналізу процесу та випуск в режимі реального часу
Традиційне тестування якості відбувається в окремих кінцевих точках партії. Технологія аналізу процесів дозволяє здійснювати безперервний моніторинг критично важливих атрибутів якості під час виробництва.
Збір даних у режимі реального часу сприяє швидшому прийняттю рішень і виявленню відхилень до того, як вони погіршать якість продукту. Деякі передові підприємства впроваджують тестування релізу в режимі реального часу, коли дані безперервного моніторингу замінюють тестування кінцевого продукту, що значно скорочує терміни випуску.
Цифрові близнюки та оптимізація лікування за допомогою штучного інтелекту
Технологія цифрових двійників створює віртуальні копії біологічних систем, уможливлюючи моделювання та прогнозування до фізичного втручання. Для клітинної та генної терапії цифрові двійники працюють на різних рівнях.
Цифрові двійники на рівні пацієнта
Дослідження, опубліковані в медичних журналах, демонструють, що цифрові двійники можуть прогнозувати результати клітинної терапії CAR-T шляхом інтеграції геномних даних, результатів візуалізації, інформації з датчиків, що носяться, та клінічних записів у багатомасштабні симуляції.
Ці моделі, орієнтовані на конкретного пацієнта, допомагають лікарям:
- Прогнозування відповіді на лікування на основі індивідуальних характеристик пухлини та імунного профілю
- Оптимізуйте стратегії дозування, щоб збалансувати ефективність та ризики токсичності
- Визначити пацієнтів, які, найімовірніше, отримають користь від конкретних терапевтичних підходів
- Моніторинг реакції після лікування та виявлення ранніх сигналів рецидиву
Алгоритми машинного навчання, навчені на історичних даних пацієнтів, з часом покращують точність прогнозування. Зі збільшенням наборів даних цифрові двійники стають все більш точними у прогнозуванні індивідуальних траєкторій лікування.
Виробничий процес Цифрові двійники
Окрім догляду за пацієнтами, цифрові двійники моделюють виробничі процеси. Віртуальні виробничі симуляції визначають оптимальні параметри процесу, прогнозують вихід продукції та тестують зміни в процесі, не використовуючи реальний матеріал пацієнта.
Ця здатність виявляється особливо цінною під час трансферу технологій - при переміщенні процесів між об'єктами розробки та комерційного виробництва або при масштабуванні від малих до великих обсягів виробництва.
Інновації в клінічних дослідженнях за допомогою цифрових технологій
Цифрові технології трансформують способи розробки, проведення та моніторингу клінічних випробувань, що особливо важливо з огляду на обмеженість популяцій пацієнтів для багатьох показань до ТГТ.
Компоненти децентралізованого судового розгляду
Хоча для проведення КГТ потрібні спеціалізовані приміщення, цифрові інструменти дозволяють здійснювати віддалений моніторинг пацієнтів, віртуальні консультації та забір зразків на дому, де це доцільно.
Носимі пристрої відстежують параметри безпеки безперервно, а не під час окремих візитів до клініки. Результати, про які повідомляють пацієнти, надходять безпосередньо в бази даних випробувань через мобільні додатки. Телемедичні платформи дають змогу часто відвідувати лікарів без зайвих витрат на переїзди.
Інтеграція реальних даних
Американське товариство генної та клітинної терапії нещодавно подало коментарі на підтримку стандартів швидкої взаємодії ресурсів охорони здоров'я сьомого рівня (HL7 FHIR) для інтеграції даних у реальному світі.
Реальні дані, отримані з електронних медичних карток, страхових відшкодувань і реєстрів пацієнтів, доповнюють традиційну інформацію про клінічні випробування, надаючи уявлення про довгострокову безпеку, ефективність у широких верствах населення та порівняльні результати лікування.
FDA вивчає можливості включення реальних даних у процес прийняття регуляторних рішень, зокрема, для моніторингу безпеки після схвалення та розширення етикетки.
Адаптивні дослідні зразки
Цифрові платформи даних уможливлюють адаптивні дизайни випробувань, які модифікують протоколи на основі накопичених доказів. Для рідкісних захворювань з обмеженою популяцією пацієнтів адаптивні підходи максимізують збір інформації, мінімізуючи вплив на пацієнтів неефективних методів лікування.
Ранні фази випробувань все частіше поєднують цілі фаз 1 і 2, фокусуючись одночасно на безпеці та попередній ефективності. Такий оптимізований підхід є науково обґрунтованим та етично прийнятним з огляду на нагальні незадоволені потреби.
Регуляторні міркування та механізми дотримання вимог
Цифрова трансформація повинна відповідати очікуванням регуляторних органів, що змінюються. FDA випустило рекомендації щодо передових виробничих технологій, штучного інтелекту в медичних пристроях і цифрових технологій охорони здоров'я в клінічних випробуваннях.
Позначення передових технологій виробництва
У грудні 2024 року FDA опублікувало остаточне керівництво для Програми призначення передових виробничих технологій. Ця програма дозволяє виробникам подавати заявки на реєстрацію конкретних технологій, які можуть покращити якість продукції, зменшити виробничі ризики або вирішити проблему дефіциту лікарських засобів.
Відібрані технології отримують розширену взаємодію з FDA, включаючи зустрічі для обговорення планів розвитку, оцінки виробництва та шляхів регуляторного регулювання. Така проактивна співпраця допомагає організаціям впроваджувати нові технології, зберігаючи при цьому відповідність нормативним вимогам.
Цілісність даних та перевірка системи
Цифрові системи повинні відповідати суворим вимогам до цілісності даних. Електронні записи повинні мати аудиторські сліди, що документують створення, модифікацію та видалення всіх даних. Доступ до системи вимагає контролю на основі ролей і регулярного перегляду.
Валідація комп'ютерних систем демонструє, що цифрові платформи стабільно працюють за призначенням. Протоколи валідації документують системні вимоги, процедури тестування та постійного моніторингу, створюючи докази того, що системи підтримують цілісність даних протягом усього свого життєвого циклу.
Нагляд за ШІ та машинним навчанням
У міру того, як технології штучного інтелекту впроваджуються в розробку і виробництво ПГТ, адаптується і регуляторна база. FDA визнає, що системи AI/ML включають “складні та динамічні процеси”, які вимагають інших підходів до нагляду, ніж традиційне програмне забезпечення.
Ключовими факторами є прозорість алгоритму, репрезентативність навчальних даних, моніторинг продуктивності під час розгортання та процедури контролю змін, коли моделі оновлюються на основі нових даних.
Подолання бар'єрів на шляху впровадження
Незважаючи на очевидні переваги, цифрова трансформація стикається з перешкодами. Розуміння загальних бар'єрів допомагає організаціям розробити стратегії їх подолання.
Культурний та організаційний опір
Перехід від паперового документообігу до цифрових систем вимагає культурних змін. Персонал, який звик до традиційних процесів, може чинити опір новим підходам - особливо, якщо навчання є недостатнім або переваги не були чітко роз'яснені.
Успішне впровадження ставить на перше місце управління змінами:
- Залучайте кінцевих користувачів до вибору технології та розробки робочого процесу
- Забезпечити комплексне навчання з можливістю практичних занять
- Визначте та наділіть повноваженнями цифрових чемпіонів у кожній функціональній сфері
- Святкуйте перші перемоги та широко діліться історіями успіху
- Прозоро вирішувати проблеми та коригувати впровадження на основі зворотного зв'язку
Складність системної інтеграції
Організації CGT працюють з багатьма спеціалізованими системами - системами управління виробництвом, лабораторними інформаційними системами, платформами планування ресурсів підприємства, системами управління клінічними випробуваннями тощо.
Створення безперебійного потоку даних між цими системами вимагає ретельної інтеграційної архітектури. Інтерфейси прикладного програмування забезпечують зв'язок між системами, але інтеграційні проекти вимагають значних технічних ресурсів і тестування.
Багато організацій застосовують поетапні підходи - спочатку надають пріоритет інтеграції, що має найбільшу цінність, а не намагаються одразу здійснити всеохоплююче з'єднання.
Обмеженість ресурсів та невизначеність рентабельності інвестицій
Цифрова трансформація вимагає попередніх інвестицій у програмне забезпечення, інфраструктуру, консультаційні послуги та час персоналу. Для невеликих організацій або тих, що розробляють методи лікування надрідкісних захворювань, обмеженість ресурсів може затримати або унеможливити впровадження.
Створення чітких бізнес-кейсів допомагає забезпечити фінансування. Кількісна оцінка очікуваних переваг - скорочення тривалості циклу, зниження рівня помилок, підвищення прибутковості, пришвидшення подання документів до регуляторних органів - створює реальні прогнози рентабельності інвестицій, які виправдовують інвестиції.
Хмарні моделі програмного забезпечення як послуги зменшують початкові потреби в капіталі порівняно з локальними системами, роблячи цифрові інструменти доступнішими для організацій з обмеженим бюджетом.
| Зона викликів | Загальні бар'єри | Стратегії пом'якшення наслідків |
|---|---|---|
| Вибір технології | Переважна кількість постачальників, нечітка диференціація функцій | Спочатку визначте вимоги, проведіть пілотний проект перед повною віддачею, зверніться за рекомендаціями до колег |
| Міграція даних | Проблеми з якістю застарілих даних, несумісність форматів | Проактивне очищення даних, створення протоколів перевірки міграції, прийняття поетапного підходу |
| Дотримання нормативних вимог | Невизначеність щодо вимог до валідації, проблеми з готовністю до аудиту | Залучайте регуляторні органи на ранніх стадіях, використовуйте пакети перевірки постачальників, ретельно документуйте |
| Навчання персоналу | Обмеженість у часі, різний рівень технічної підготовки | Рольові навчальні траєкторії, модель суперкористувача, постійні ресурси підтримки |
| Управління постачальниками | Відносини з багатьма постачальниками, інтеграційні залежності | Надавайте пріоритет платформам з відкритими API, встановлюйте чітке управління, ведіть картки оцінки постачальників |
Глобальна доступність та справедливість у сфері охорони здоров'я
Цифрова трансформація повинна враховувати глобальні проблеми доступності. Трансляція клітинної та генної терапії в країни з низьким та середнім рівнем доходу стикається зі значними бар'єрами.
У період з 1991 по 2008 рік лише близько 21 ТП3Т з 274 000 глобальних клінічних випробувань було проведено в Африці, незважаючи на те, що цей континент несе значний тягар захворювань. Обмеженість регуляторного потенціалу, прогалини в інфраструктурі та нестача ресурсів ускладнюють доступ до передових методів лікування.
Цифрові технології пропонують часткові рішення:
- Платформи телемедицини дають змогу дистанційно консультуватися з фахівцями без дорогих поїздок
- Хмарні регуляторні системи зменшують вимоги до локальної інфраструктури
- Спільні виробничі мережі можуть ефективно обслуговувати кілька регіонів
- Цифрові навчальні програми розбудовують місцевий потенціал, не вимагаючи особистих поїздок експертів
Однак самі по собі технології не вирішують проблеми фундаментальної нерівності в доступі до охорони здоров'я, механізмах фінансування та промислових потужностях. Цифрова трансформація має доповнювати, а не замінювати ширші зусилля, спрямовані на демократизацію доступу до передової терапії в усьому світі.
Майбутні напрямки та нові технології
Цифрові інновації в галузі ПГТ продовжують прискорюватися. Кілька нових технологій є особливо перспективними.
Блокчейн для перевірки ланцюгів поставок
Технологія розподіленого реєстру блокчейн створює незмінні записи про поводження з продуктами, умови зберігання та передачу прав власності. Для аутологічної терапії, що вимагає абсолютної гарантії ідентичності, блокчейн пропонує криптографічно підтверджену відстежуваність.
Перші впровадження демонструють доцільність, хоча широке впровадження чекає на стандартизацію та інтеграцію з існуючими системами.
Розширена аналітика та прогнозоване виробництво
Моделі машинного навчання, навчені на історичних виробничих даних, можуть прогнозувати результати партій, виявляти відхилення в процесі до того, як вони вплинуть на якість, і рекомендувати коригування параметрів для оптимізації виходу продукції.
Зі збільшенням наборів виробничих даних покращуються можливості прогнозування, що потенційно може дозволити виробництво з мінімальним втручанням людини на рутинних виробничих етапах.
Синтетична біологія та комп'ютерний дизайн
Обчислювальні інструменти прискорюють розробку інженерної клітинної терапії. Замість емпіричного методу спроб і помилок, підходи синтетичної біології використовують моделювання для розробки генетичних схем, прогнозування поведінки клітин та оптимізації терапевтичних конструкцій in silico перед фізичним тестуванням.
Ця можливість комп'ютерного дизайну доповнює цифрові двійники - разом вони створюють комплексне віртуальне середовище для розробки та оптимізації терапії.
Дорожня карта практичної реалізації
Організації, які починають цифрову трансформацію, повинні дотримуватися структурованих підходів, а не впроваджувати технології від випадку до випадку.
Крок 1: Оцініть поточний стан
Задокументуйте існуючі процеси, системи та потоки даних. Визначте больові точки, неефективність та комплаєнс-ризики. Оцініть цифрову зрілість виробничих, якісних, клінічних та комерційних функцій.
Крок 2: Визначте стратегічне бачення
Встановіть чіткі цілі, узгоджені з бізнес-пріоритетами. Яких конкретних результатів має досягти цифрова трансформація? Скорочення часу виходу на ринок? Покращення якості продукції? Кращі результати для пацієнтів? Зниження виробничих витрат?
Визначте пріоритетність кейсів використання на основі очікуваного впливу та можливості реалізації.
Крок 3: Виберіть відповідні технології
Оцініть платформи відповідно до визначених вимог. Враховуйте можливості інтеграції, стабільність постачальника, відповідність нормативним вимогам, масштабованість та загальну вартість володіння.
Уникайте підходів, орієнтованих на технологію, які обирають інструменти до того, як зрозуміють потреби.
Крок 4: Виконайте сфокусовані пілотні проекти
Тестуйте обрані технології в контрольованих масштабах перед розгортанням в масштабах всієї організації. Пілотні проекти підтверджують очікувані переваги, виявляють проблеми впровадження та зміцнюють довіру в організації.
Документуйте отримані уроки та вдосконалюйте підходи перед масштабуванням.
Крок 5: Масштабування успішних ініціатив
Розширюйте перевірені пілотні проекти на інші сайти, продукти чи функції. Інвестуйте в навчання, управління змінами та постійну інфраструктуру підтримки.
Створити систему управління, що забезпечує послідовне розгортання та запобігає несанкціонованим модифікаціям системи.
Крок 6: Оптимізуйте безперервно
Відстежуйте показники ефективності, збирайте відгуки користувачів та ітеративно вдосконалюйте процеси. Цифрова трансформація - це не одноразовий проєкт, а постійний процес, що потребує постійної уваги.
Будьте в курсі нових технологій та регуляторних очікувань за допомогою галузевих асоціацій, конференцій та мереж колег.
| Етап впровадження | Типова тривалість | Основні результати | Показники успіху |
|---|---|---|---|
| Оцінка | 1-2 місяці | Документація поточного стану, аналіз прогалин, оцінка зрілості | Всебічне розуміння базових можливостей |
| Розробка стратегії | 1-2 місяці | Формулювання бачення, пріоритетні варіанти використання, дорожня карта, бізнес-кейс | Виконавче узгодження та затвердження фінансування |
| Вибір технології | 2-3 місяці | Документ з вимогами, оцінка постачальників, рішення про вибір | Вибір платформи відповідає вимогам |
| Пілотне виконання | 3-6 місяців | Налаштована система, навчені користувачі, результати пілотного проекту, отримані уроки | Перевірені переваги, вдосконалений підхід до впровадження |
| Масштабне розгортання | 6-18 місяців | Розгортання на підприємстві, розширене навчання, завершення інтеграції | Цілі впровадження, покращення продуктивності |
| Безперервна оптимізація | Триває | Панелі моніторингу ефективності, регулярні огляди, відставання у вдосконаленні | Сталі переваги, задоволеність користувачів, можливості, що розвиваються |
Створення надійної цифрової основи для клітинної та генної терапії
Робота в галузі клітинної та генної терапії залежить від точних даних, процесів, які можна відстежити, та систем, які можуть обробляти як дослідження, так і виробництво, не порушуючи безперервності. Програмне забезпечення A-list підтримує організації, вивчаючи, як наразі структуровані дані, системи та робочі процеси, а потім реорганізовує їх для покращення узгодженості та контролю.
Це часто включає вдосконалення способів зберігання інформації та доступу до неї, скорочення ручної передачі даних і забезпечення здатності систем підтримувати зростання без створення розривів між етапами роботи. Якщо ваші поточні налаштування ускладнюють контроль або безпечне масштабування, зверніться до Програмне забезпечення списку А щоб отримати чітке, практичне уявлення про те, як рухатися далі.
Вимірювання успіху цифрової трансформації
Кількісні показники демонструють цінність трансформації та спрямовують на постійне вдосконалення.
Виробничі показники включають скорочення часу циклу, показники успішності партії, частоту відхилень і час до випуску. Провідні організації повідомляють про 20-40% покращення в цих сферах після оцифрування.
Показники якості відстежують рівень помилок, терміни розслідування, результати аудиту та результати перевірок. Електронні системи зазвичай зменшують кількість помилок у документації на 60-80% порівняно з паперовими процесами.
Клінічні показники вимірюють швидкість набору пацієнтів, частоту відхилень від протоколу, показники якості даних та ефективність моніторингу. Цифрові інструменти можуть скоротити терміни набору на 30% або більше.
Фінансові показники включають витрати на партію, балансову вартість запасів, продуктивність праці та рентабельність цифрових інвестицій. Комплексні трансформації зазвичай досягають позитивної рентабельності інвестицій протягом 18-36 місяців.
Поширені запитання
- Які найбільші виклики у виробництві клітинної та генної терапії, що трансформуються за допомогою цифрових технологій?
Основні виклики включають складність системної інтеграції між кількома спеціалізованими платформами, культурний опір персоналу, який звик до паперового документообігу, ресурсні обмеження, що обмежують початкові інвестиції, невизначеність щодо відповідності новим технологіям нормативним вимогам та міграцію даних зі старих систем. Організації долають ці бар'єри завдяки поетапному впровадженню, ефективному управлінню змінами, чіткій демонстрації рентабельності інвестицій та завчасному залученню регуляторних органів.
- Як цифрові двійники покращують результати клітинної терапії CAR-T?
Цифрові двійники створюють віртуальні моделі пацієнтів, інтегруючи геномні дані, характеристики пухлини, імунні профілі, результати візуалізації та клінічну історію. Ці різномасштабні симуляції прогнозують індивідуальну відповідь на лікування, оптимізують стратегії дозування, визначають пацієнтів, які, найімовірніше, отримають користь від лікування, і дають змогу на ранніх стадіях виявляти сигнали рецидиву. Алгоритми машинного навчання підвищують точність прогнозування в міру розширення наборів даних, що робить цифрових двійників все більш цінними для персоналізації терапевтичних підходів.
- Яке нормативне регулювання існує для передових виробничих технологій у ПГУ?
У грудні 2024 року FDA завершило розробку інструкцій, що запроваджують Програму призначення передових виробничих технологій. Ця програма дозволяє виробникам подавати заявки на реєстрацію технологій, які покращують якість, знижують ризики або усувають дефіцит. Відібрані технології отримують посилену підтримку FDA, включаючи зустрічі з розробниками та обговорення шляхів регулювання. Додаткові рекомендації стосуються ШІ/МЛ у медичних виробах, цифрових технологій у сфері охорони здоров'я у випробуваннях та вимог до цілісності даних для електронних систем.
- Скільки часу зазвичай займає цифрова трансформація для організацій клітинної та генної терапії?
Часові рамки варіюються залежно від масштабу та організаційної готовності. Початкова оцінка та розробка стратегії потребують 2-4 місяці. Вибір технології додає 2-3 місяці. Пілотні проекти тривають 3-6 місяців. Розгортання в масштабах підприємства займає 6-18 місяців для комплексної трансформації. Однак організаціям слід розглядати це як безперервну еволюцію, а не як кінцеві проекти - постійна оптимізація триває нескінченно довго, оскільки технології та потреби розвиваються.
- Чи можуть невеликі біотехнологічні компанії дозволити собі ініціативи з цифрової трансформації?
Так, хоча підходи відрізняються від підходів великих фармацевтичних компаній. Хмарні платформи програмного забезпечення як послуги зменшують вимоги до капіталу порівняно з локальними системами. Сфокусовані впровадження, орієнтовані на найвигідніші варіанти використання, дають переваги без комплексного розгортання на підприємстві. Організації, що займаються розробкою та виробництвом за контрактом, все частіше пропонують цифрові послуги, що дозволяє невеликим компаніям отримати доступ до розширених можливостей без розбудови внутрішньої інфраструктури. Поетапні підходи розподіляють витрати в часі, забезпечуючи при цьому додаткову цінність.
- Як оцифрування покращує управління ланцюгами поставок для аутологічної терапії?
Цифрові платформи ланцюгів поставок об'єднують в єдині системи планування роботи пунктів збору, відстеження логістики, оновлення статусу виробництва та координацію роботи центрів обробки. Прозорість у реальному часі дозволяє проактивно управляти винятковими ситуаціями, а не реагувати на них. Системи ідентифікації, що використовують біометричну верифікацію, RFID-мітки та сканування штрих-кодів, забезпечують відстеження продукту від аферезу до інфузії. Моніторинг температури, оптимізація маршрутів і автоматизоване документування зменшують кількість помилок, одночасно прискорюючи час переливання з вени в вену на 15-30%.
- Яку роль відіграють реальні дані у розвитку клітинної та генної терапії?
Реальні дані з електронних медичних карток, баз даних претензій і реєстрів пацієнтів дають уявлення про довгострокову безпеку, ефективність у різних групах населення та порівняльні результати лікування поза межами контрольованих випробувань. FDA розробляє механізми для включення реальних даних у регуляторні рішення, зокрема, для післяреєстраційного моніторингу безпеки, розширення етикетки та рідкісних захворювань, де традиційні випробування стикаються з проблемами набору пацієнтів. Стандартизовані формати даних, такі як HL7 FHIR, дозволяють ефективно інтегрувати реальні дані в програми розвитку.
Висновок
Цифрова трансформація - це більше, ніж просто впровадження технологій, це фундаментальне переосмислення того, як розробляються, виробляються та доставляються пацієнтам клітинні та генні терапії.
Від прогнозування лікування на основі штучного інтелекту до автоматизованих виробничих платформ - цифрові інструменти вирішують критичні проблеми, що обмежують масштабованість і доступність ХГТ. Організації, які впроваджують ці технології, повідомляють про скорочення термінів розробки, підвищення якості продукції, зниження витрат і поліпшення результатів лікування пацієнтів.
Проте сама по собі технологія не гарантує успіху. Ефективна трансформація вимагає стратегічного бачення, міжфункціональної співпраці, узгодження з регуляторними нормами, управління змінами та постійної оптимізації. Організації повинні балансувати між інноваціями та дотриманням вимог, швидкістю та якістю, автоматизацією та людським наглядом.
Підтримка FDA передових виробничих технологій за допомогою програм реєстрації та розширеного залучення створює сприятливе регуляторне середовище для інновацій. З розвитком цифрових можливостей і розширенням їх застосування клітинна та генна терапія все більше виконуватиме свої обіцянки щодо лікування раніше невиліковних станів.
Настав час для організацій КГТ оцінити цифрову зрілість, визначити цінні можливості та розпочати шлях до трансформації. Конкурентні переваги - і переваги для пацієнтів - роблять цифрову трансформацію не просто корисною, а необхідною.
Готові до цифрової трансформації вашої організації? Почніть з оцінки поточних можливостей у порівнянні з галузевими стандартами, визначення больових точок з вимірюваним впливом на бізнес та пріоритизації ініціатив, які дають швидкі результати, одночасно рухаючись до всеосяжних змін.


